Ch3 это что: Спирты — химические свойства, формулы и получение
Содержание
Амины — что это? | Химтраст
-
О компании- О компании
- Дилерская политика
- Вакансии
- Новости
- Отзывы
- Сертификаты
- Благотворительность
- Специальная оценка условий труда
-
Каталог -
Скидки -
Покупателям- Калькулятор
- Правила оплаты
- Контакты дилеров
-
Услуги- Теплоизоляция
- Гидроизоляция
- Огнезащита
- Укладка резиновой крошки
- Заливка наливных полов
- Фотоотчеты
-
База знаний- Статьи
- Альбом решений
- Видео
- Вопросы и ответы
- Энциклопедия
-
Обучение- Курс напыленщиков
- Курс по работе с оборудованием PROTON
-
Контакты
-
-
Каталог
Калькулятор напылёнщика
Рассчитайте толщину напыления и объем компонентов ППУ
перейти к калькулятору
Аминами называются органические производные аммиака, в котором один, два или все три атома водорода замещены на углеводородные радикалы (предельные, непредельные, ароматические). Название аминов производят от названия углеводородного радикала с добавлением окончания –амин или от названия соответствующего углеводорода с приставкой амино-.
Название аминов производят от названия углеводородного радикала с добавлением окончания –амин или от названия соответствующего углеводорода с приставкой амино-.
Примеры:
-
Ch4 – Nh3 — метиламин; - Ch4 – NH – C2H5 — метилэтиламин.
фениламин (анилин)
В зависимости от числа атомов водорода, замещенных в аммиаке на углеводородные радикалы, различают первичные, вторичные и третичные амины:
- первичный амин: R – Nh3
- вторичный амин: R – NH – R’
- третичный амин: R – N – R”
Где R, R’, R’’ – углеводородные радикалы.
Первичные, вторичные и третичные амины можно получить, проводя алкилирование (введение алкильного радикала) аммиака. При этом происходит постепенное замещение атомов водорода аммиака на радикалы, и образуется смесь аминов:
-
Nh4 + Ch4I — Ch4Nh3 + HI -
Ch4Nh3 + Ch4I — (Ch4)2NH + HI -
(Ch4)2NH + Ch4I — (Ch4)2N + HI
Обычно в смеси аминов преобладает один из них в зависимости от соотношения исходных веществ.
Для получения вторичных и третичных аминов можно использовать реакцию аминов с галогеналкилами:
(Ch4)2NH + C2H5Br — (Ch4)2NC2H5 + HBr
Амины можно получить восстановлением нитросоединений. Обычно нитросоединения подвергают каталитическому гидрированию водородом:
C2H5NO2 + 3h3 — C2H5Nh3 + 2h3O
Этот метод используется в промышленности для получения ароматических аминов.
Предельные амины. При обычных условиях метил амин Ch4Nh3, диметиламин (Ch4)2NH, триметиламин (Ch4)3N и этиламин C2H5Nh3 – газы с запахом, напоминающим запах аммиака. Эти амины хорошо растворимы в воде. Более сложные амины – жидкости, высшие амины – твердые вещества.
Для аминов характерны реакции присоединения, в результате которых образуются алкиламиновые соли. Например, амины присоединяют галогеноводороды:
(Ch4)2Nh3 +HCl — [(Ch4)2Nh4]Cl
хлорид этиламмония
(Ch4)2NH + HBr — [(Ch4)2Nh3]Br
бромид диметиламмония
(Ch4)3N + HI — [(Ch4)3NH]I
иодид триметиламмония
Тритичные амины присоединяют галогенопроизводные углеводорода с образованием тетраалкиламмониевых солей, например:
(C2H5)3N + C2H5I — [(C2H5)4N]I
Алкиламониевые соли растворимы в воде и в некоторых органических растворителях.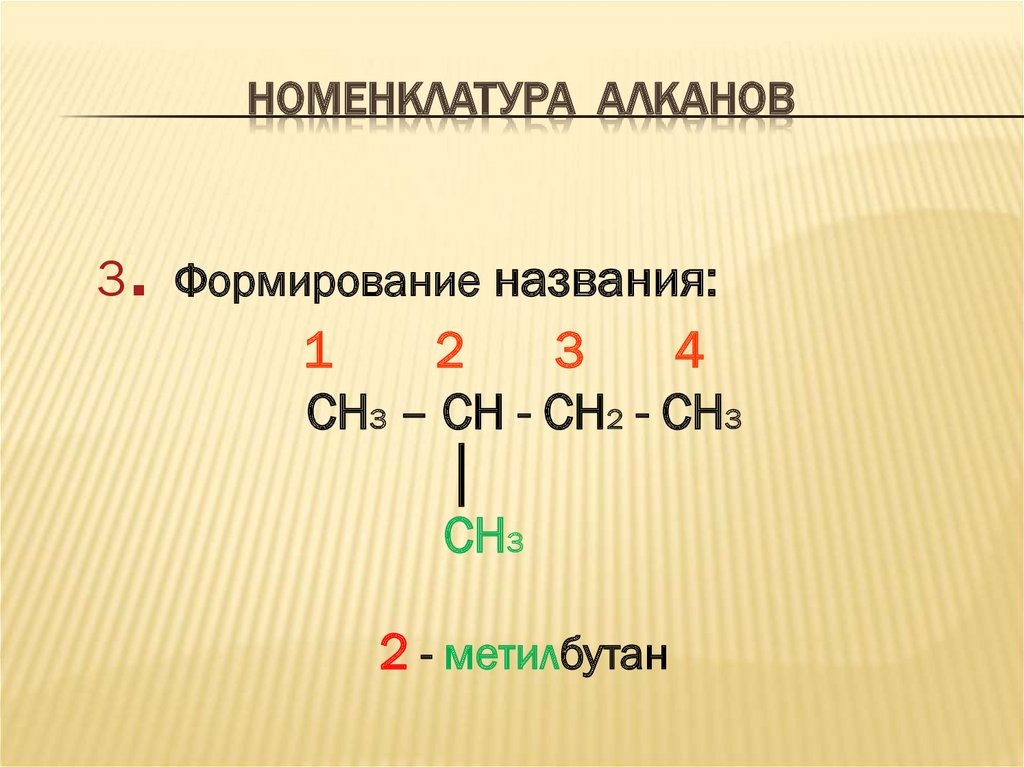 При этом они диссоциируют на ионы:
При этом они диссоциируют на ионы:
[(C2H5)4N]I === [(C2H5)4N]+ + I-
В результате водные и неводные растворы этих солей проводят электрический ток. Химическая связь в алкиламмониевых соединениях ковалентная, образованная по донорно-акцепторному механизму:
Ион метиламмония
Метил | это… Что такое Метил?
Метил
Метил — это одновалентный радикал метана. Следует отделять частицу — свободный радикал ·CH3 (частица с неспаренным электроном на внешней орбитали) и группу атомов — метильная группа -CH3 (также обозначается как -Ме), являющейся частью химического соединения.
Содержание
|
Метильный радикал
Время жизни — 0. 0084 секунд (в токе водорода и при разряжении 1-2 мм рт.ст.)[1], но его можно уменьшить или продлить при помощи катализаторов или ингибиторов.
0084 секунд (в токе водорода и при разряжении 1-2 мм рт.ст.)[1], но его можно уменьшить или продлить при помощи катализаторов или ингибиторов.
Химически крайне активен, легко димеризуется с образованием этана
- CH3· + ·CH3 → CH3-CH3
Образуется в свободном виде при некоторых реакциях:
- при распаде тетраметилсвинца
- Pb(CH3)4 →(t) Pb + 4CH3·
- при распаде некоторых азосоединений (содержат группу -N=N-)
- электролизе водных растворов ацетатов (на аноде)
- CH3COO− — e− → CH3COO·
- CH3COO· → CH3· + CO2↑
- при реакции хлорирования[2], нитрования, окисления метана
- Cl2 (hν или)→ 2Cl·
- Cl· + CH4 → HCl + CH3·
Используется в химической промышленности при синтезе метанола, формальдегида, применяется для изготовления некоторых лекарств, ядов (формальдегид), полимерных тканей (дегидрирование, полиметилен)
Метильная группа
Является заместителем во множестве органических соединениях. Также терминальный заместитель в углеводородах Введение метильной группы может осуществляется:
Также терминальный заместитель в углеводородах Введение метильной группы может осуществляется:
- по реакции SN2 замещения при использовании иодметана, диметилсульфата, метилтозилата.
- Et2NH + MeI → Et2NMe*HI
- при реакции соединений с электрофильными группами (С-Hal, С=O, -CN) с металлорганическими соединениями (MeMgCl, Zn(CH3)2)
- Me2CO + MeMgCl → Me3C-O-MgCl
- по радикальному механизму, в частности, при реакции с диазометаном
- RCOOH + CH2N2 → RCOOCH3 + N2
- в биохимических процессах осуществляется переносом метилтрансферазами с S-аденозилметионина [3] на субстрат
Введение в соединение метильной группы увеличивает липофильность вещества.
Активность метильной группы определяется группой атомов к которой она присоединена. В алканах она крайне малоактивна.
Донаторы метила для омоложения организма
Примечания
- ↑ Берберова Н. Т. Из жизни свободных радикалов, ХИМИЯ 2000
- ↑ Хлорирование метана
- ↑ S-АДЕНОЗИЛМЕТИОНИН
См. также
- Метилирование
- Дистаннан
Углеводороды
Углеводороды
Углеводороды
Органические молекулы:
Органическая химия изучает свойства соединений углерода. Все соединения углерода, за исключением нескольких неорганических соединений углерода, являются органическими. Неорганические соединения углерода включают оксиды углерода, бикарбонаты и карбонаты ионов металлов, цианиды металлов и некоторые другие.
Углеводороды
Простейшие органические соединения состоят только из атомов углерода и водорода. Соединения только углерода и водорода называются Углеводороды .
Алканы
Простейший углеводород – метан, CH 4 . Это простейший член ряда углеводородов. Каждый последующий член ряда имеет на один атом углерода больше, чем предыдущий член. Этот ряд соединений называется алканов ( С n H 2n+2 ) . Более легкие газы и используются в качестве топлива. Средние (от 7 углеродов до 12 углеродов) — это жидкости, используемые в бензине (бензине). Высшие представляют собой воскообразные твердые вещества. Свечной воск представляет собой смесь алканов. Алканы являются насыщенными, что означает, что они содержат максимальное количество атомов водорода на углерод и не содержат двойных или тройных связей.
Это простейший член ряда углеводородов. Каждый последующий член ряда имеет на один атом углерода больше, чем предыдущий член. Этот ряд соединений называется алканов ( С n H 2n+2 ) . Более легкие газы и используются в качестве топлива. Средние (от 7 углеродов до 12 углеродов) — это жидкости, используемые в бензине (бензине). Высшие представляют собой воскообразные твердые вещества. Свечной воск представляет собой смесь алканов. Алканы являются насыщенными, что означает, что они содержат максимальное количество атомов водорода на углерод и не содержат двойных или тройных связей.
Наименование органических соединений относится к органической номенклатуре . Существует множество правил именования органических соединений, систематизированных Международным союзом теоретической и прикладной химии 9.0003
Правила ИЮПАК для номенклатуры алканов
1.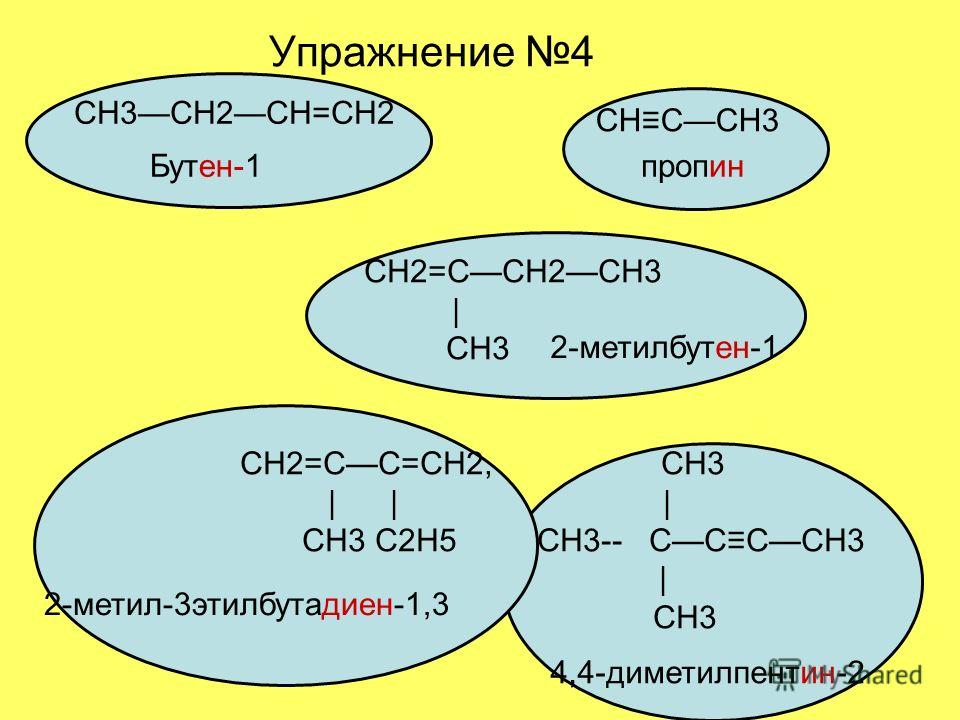 Найдите и назовите самую длинную непрерывную углеродную цепь.
Найдите и назовите самую длинную непрерывную углеродную цепь.
2. Определите и назовите группы, присоединенные к этой цепочке.
3. Последовательно пронумеруйте цепь, начиная с конца, ближайшего к группе заместителей.
4. Обозначьте расположение каждой группы заместителей соответствующим номером и названием.
5. Соберите название, перечислив группы в алфавитном порядке.
Приставки ди, три, тетра и т. д., используемые для обозначения нескольких однородных групп, при алфавитном алфавите не учитываются.
Количество атомов углерода | Префикс | Структура |
1 | Мет ан | CH 4 |
2 | Эт ан | CH 3 CH 3 |
3 | Опора ан | CH 3 CH 2 CH 3 |
4 | Бут ане | CH 3 (CH 2 ) 2 CH 3 |
5 | Пент ан | CH 3 (CH 2 ) 3 CH 3 |
6 | Шестигранник Ане | Ч 3 (CH 2 ) 4 CH 3 |
7 | Гепт ане | CH 3 (CH 2 ) 5 CH 3 |
8 | октябрь ан | CH 3 (CH 2 ) 6 CH 3 |
9 | Не ан | CH 3 (CH 2 ) 7 CH 3 |
10 | декабрь ан | CH 3 (CH 2 ) 8 CH 3 |
11 | Ундец ан | CH 3 (CH 2 ) 9 CH 3 |
12 | Додек ане | CH 3 (CH 2 ) 10 CH 3 |
Изомерия
Все алканы с 4 и более атомами углерода проявляют структурную изомерию .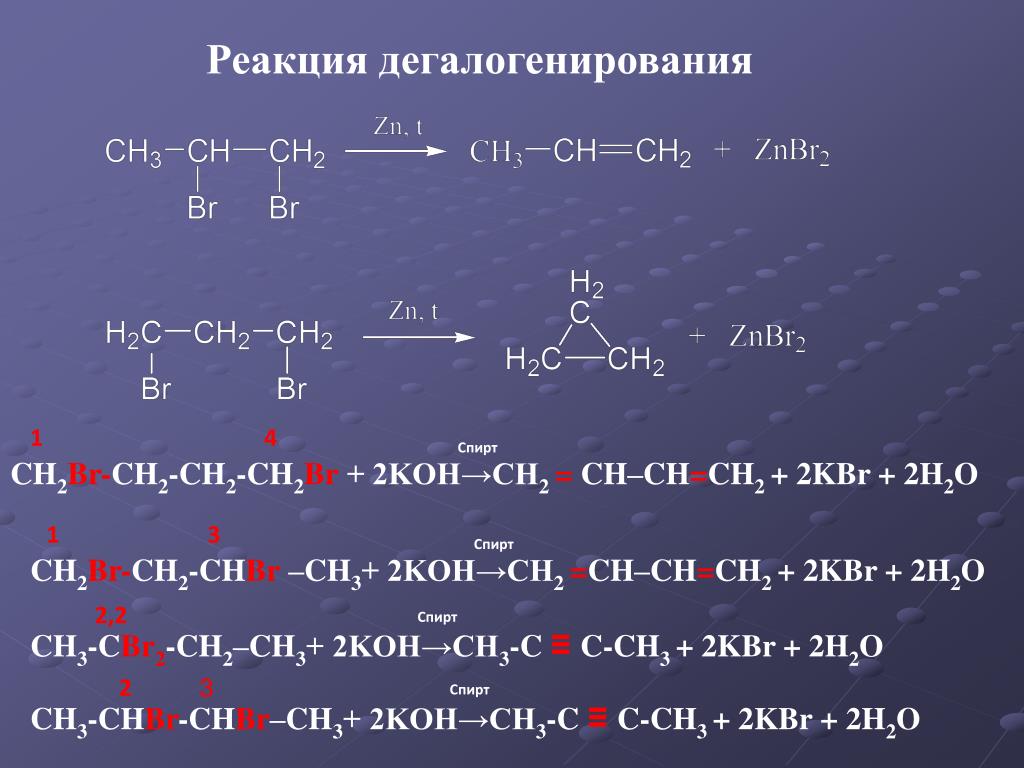 Это означает, что для каждой молекулярной формулы можно нарисовать две или более различных структурных формул.
Это означает, что для каждой молекулярной формулы можно нарисовать две или более различных структурных формул.
Например, C 4 H 10 может быть любой из этих двух разных молекул:
Они называются соответственно бутан и 2-метилпропан .
Наименование структурных изомеров алканов
Номенклатура усложняется, если алкан разветвляется. В таком случае есть несколько правил, которым вы должны следовать, чтобы дать алкану правильное название.
- Найдите самую длинную углеродную цепь в молекуле. Количество атомов углерода в самой длинной цепи становится родительским именем (см. таблицу выше)
- Найдя исходную цепь, вы нумеруете исходную цепь, начиная с конца, ближайшего к первому заместителю (заместителем является любой фрагмент, выступающий за пределы основной цепи).
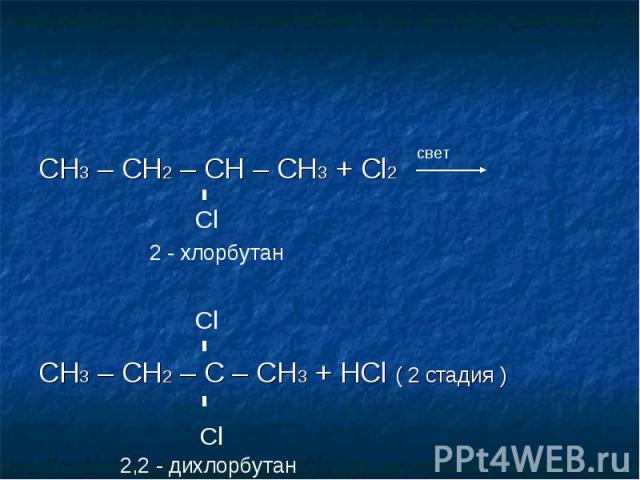
- Далее определите названия всех заместителей . Заместители называются так, как если бы часть была отдельной молекулой, за исключением того, что используется суффикс yl, а не ane. Таким образом, двухуглеродный заместитель будет этильным заместителем (а не этановым заместителем).
- Поместите заместители в алфавитном порядке (т.е. этил перед метилом) перед названием родителя.
- Затем определите положение всех заместителей в названии, поместив перед ним число атомов углерода, в котором заместитель присоединяется к исходной цепи. Например, 2-метилгептан указывает на то, что метильный заместитель присоединен к углероду номер 2.
Применение правил
Теперь попробуйте применить эти правила, чтобы назвать следующую молекулу (это не так сложно, как может показаться).
Действуйте шаг за шагом, как описано выше.
1) Найдите самую длинную углеродную цепь в молекуле. Во-первых, найдите исходную цепь в молекуле, то есть максимально длинную цепочку соединяющих атомов углерода. Обратите внимание, что родительская цепочка не обязательно является цепочкой, которая просто следует слева направо. Например, если бы вы посчитали количество атомов углерода в этой молекуле слева направо, вы бы получили 7 атомов углерода. Однако это не родительская цепочка! Если вы начнете слева, а затем подсчитаете, где молекула разветвляется, вы обнаружите, что в ней 8 атомов углерода. Это самая длинная цепь (не дайте себя обмануть профессорам, прячущим атомы углерода в ответвлениях), и, таким образом, исходной цепью является октан (см. таблицу выше).
2) Номер родительской цепочки. Второй шаг — пронумеровать атомы углерода в исходной цепи, начиная с конца, ближайшего к первому заместителю. Важно нумеровать молекулу с правильного конца (другими словами, в этом примере вы нумеруете алкан справа налево или слева направо). Следуя этому правилу, на этой молекуле вы нумеруете справа налево, так как 2-углеродный заместитель находится ближе к этому концу.
Следуя этому правилу, на этой молекуле вы нумеруете справа налево, так как 2-углеродный заместитель находится ближе к этому концу.
| | |
| Правильная нумерация | Неправильная нумерация |
3. Назовите все заместители. Затем вы определяете названия заместителей. В этом случае единственным заместителем является 2-углеродная группа у 4-го атома углерода. Это этильная группа.
4. Расположите заместители в алфавитном порядке. Следующим шагом является расположение заместителей в алфавитном порядке (т.е. этил перед метилом), но так как есть только один заместитель, в этом нет необходимости.
5. Найдите заместитель в родительском изменении, присвоив ему номер .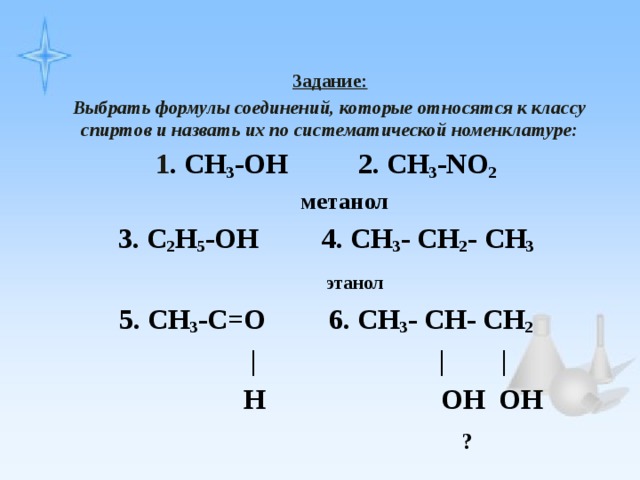 Таким образом, правильная номенклатура этого алкана — 4-этилоктан. Обратите внимание, что тире используется для отделения числа от заместителя.
Таким образом, правильная номенклатура этого алкана — 4-этилоктан. Обратите внимание, что тире используется для отделения числа от заместителя.
Циклоалканы снова содержат только углерод-водородные связи и углерод-углеродные одинарные связи, но на этот раз атомы углерода соединены в кольцо. Наименьшим циклоалканом является циклопропан.
Если вы посчитаете атомы углерода и водорода, вы увидите, что они больше не соответствуют общей формуле C n H 2n+2 . Соединяя атомы углерода в кольцо, вы должны были потерять два атома водорода.
Вряд ли он вам когда-нибудь понадобится, но общая формула циклоалкана C н Н 2 н .
Не думайте, что это все плоские молекулы. Все циклоалканы от циклопентана и выше существуют в виде «сморщенных колец».
Циклогексан
, например, имеет кольцевую структуру, которая выглядит следующим образом:
Эта форма циклогексана известна как «кресло» из-за его формы, отдаленно напоминающей стул.
Правила ИЮПАК для номенклатуры циклоалканов
1. Для монозамещенного циклоалкана кольцо дает название корня, а группа-заместитель называется, как обычно. Номер места необязателен.
2. Если алкильный заместитель большой и/или сложный, кольцо может быть названо замещающей группой алкана.
3. Если в кольце присутствуют два разных заместителя, они перечислены в алфавитном порядке, и первый указанный заместитель соответствует углероду №1. Затем нумерация атомов углерода в кольце продолжается в направлении (по часовой стрелке или против часовой стрелки), которое дает второму заместителю меньший возможный номер положения.
4. Если в кольце присутствует несколько заместителей, они перечислены в алфавитном порядке. Номера положений присваиваются заместителям таким образом, что один из них находится у углерода № 1, а другие положения имеют наименьшие возможные номера, считая либо по часовой стрелке, либо против часовой стрелки.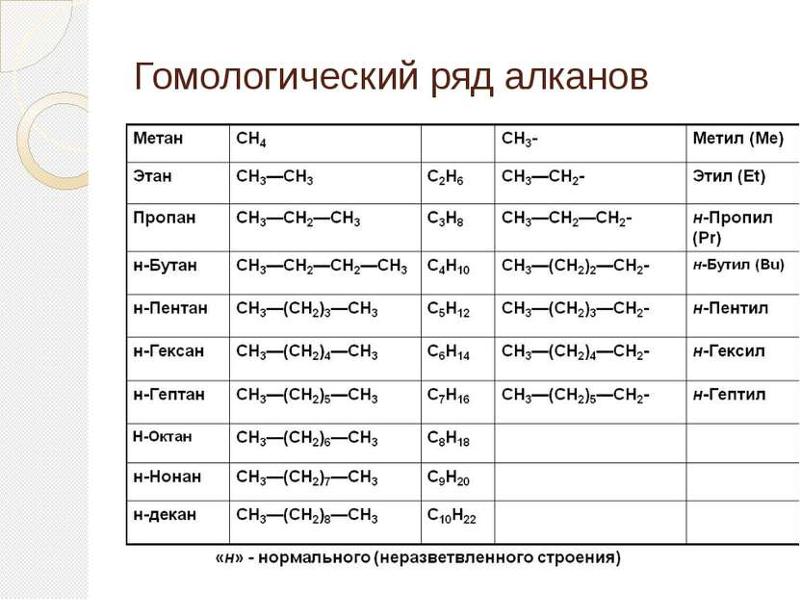
5. Название собирается, перечисляя группы в алфавитном порядке и присваивая каждой группе (если их две или более) номер местоположения. Приставки ди, три, тетра и т. д., используемые для обозначения нескольких однородных групп, при алфавитном алфавите не учитываются.
Алкены
Другая серия соединений называется алкенов . Они имеют общую формулу: C n H 2n . Алкены содержат меньше атомов водорода, чем алканы. Оставшиеся дополнительные валентности возникают в виде двойных связей между парой атомов углерода. Двойные связи более реакционноспособны, чем одинарные связи, что делает алкены химически более реакционноспособными.
Правила ИЮПАК для номенклатуры алкенов и циклоалкенов
1. Суффикс ен (окончание) указывает на алкен или циклоалкен.
2.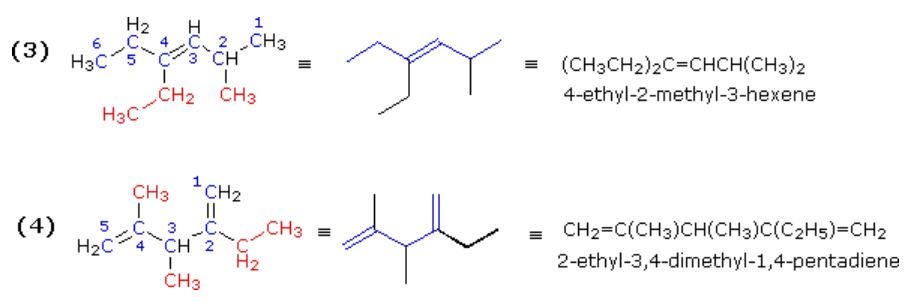 Самая длинная цепь, выбранная для корневого названия, должна включать 90 551 оба атома углерода двойной связи 90 552 .
Самая длинная цепь, выбранная для корневого названия, должна включать 90 551 оба атома углерода двойной связи 90 552 .
3. Корневая цепь должна быть пронумерована с конца, ближайшего к атому углерода двойной связи . Если двойная связь находится в центре цепи, для определения конца, с которого начинается нумерация, используется правило ближайшего заместителя.
4. Меньшее из двух чисел, обозначающих атомы углерода двойной связи, используется в качестве локатора двойной связи. Если присутствует более одной двойной связи, соединение называется диеновым, триеновым или эквивалентным префиксом, указывающим количество двойных связей, и каждой двойной связи присваивается локаторный номер.
5. В циклоалкенах атомам углерода двойной связи отведены кольцевые позиции №1 и №2. Какой из двух является номером 1, можно определить по правилу ближайшего заместителя.
6. Группы заместителей, содержащие двойные связи:
H 2 C=CH– Винильная группа
H 2 C=CH–CH 2 – Аллильная группа
Алкины
Третьей серией являются алкины . Они имеют следующую формулу: C n H 2n-2 .
Они имеют следующую формулу: C n H 2n-2 .
Алкины имеют два атома углерода, соединенных тройной связью. Это очень реакционноспособно, что делает эти соединения нестабильными.
Правила ИЮПАК для номенклатуры алкинов
1. Суффикс yne (окончание) указывает на алкин или циклоалкин.
2. Самая длинная цепь, выбранная для корневого названия, должна включать 90 551 оба атома углерода тройной связи 90 552 .
3. Корневая цепь должна быть пронумерована с конца, ближайшего к атому углерода тройной связи . Если тройная связь находится в центре цепи, для определения конца, с которого начинается нумерация, используется правило ближайшего заместителя.
4. Меньшее из двух чисел, обозначающих атомы углерода тройной связи, используется в качестве локатора тройной связи.
5. Если присутствует несколько множественных связей, каждой из них должен быть присвоен номер локатора. Двойные связи предшествуют тройным связям в названии IUPAC, но цепочка нумеруется с конца, ближайшего к кратной связи, независимо от ее природы.
Двойные связи предшествуют тройным связям в названии IUPAC, но цепочка нумеруется с конца, ближайшего к кратной связи, независимо от ее природы.
6. Поскольку тройная связь является линейной, она может быть размещена только в кольцах размером более десяти атомов углерода. В простых циклоалкинах атомам углерода тройной связи назначаются кольцевые положения № 1 и № 2. Какой из двух является номером 1, можно определить по правилу ближайшего заместителя.
7. Группы заместителей, содержащие тройные связи:
HC≡C– Этинильная группа
HC≡CH–CH 2 – Пропаргильная группа
Проблемы:
Нарисуйте структурную формулу 2-бром-4,4-дихлор-5,5-диметилгептана
Нарисуйте структурную формулу 4-бром-1-этилциклопентена
Нарисуйте структурную формулу 7-метил-6-октен-1,3-диина
14.7: Номенклатура ИЮПАК — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 218577
Цели обучения
- Называть алканы по системе ИЮПАК и писать формулы для алканов, получивших названия ИЮПАК
Как отмечалось ранее, число изомеров быстро увеличивается по мере увеличения числа атомов углерода. Имеется 3 пентана, 5 гексанов, 9 гептанов и 18 октанов. Было бы трудно присвоить уникальные индивидуальные имена, которые мы могли бы запомнить. Систематический способ именования углеводородов и других органических соединений был разработан Международным союзом теоретической и прикладной химии (IUPAC). Эти правила, используемые во всем мире, известны как Система номенклатуры IUPAC. (Некоторые названия, которые мы использовали ранее, такие как изобутан, изопентан и неопентан, не соответствуют этим правилам и называются общих имен .) Название основы (Таблица \(\PageIndex{1}\)) указывает количество атомов углерода в самой длинной непрерывной цепи (LCC). Атомы или группы, присоединенные к этой углеродной цепи, называемые заместителями , затем называются, а их положения обозначаются цифрами. Сейчас мы будем рассматривать только те заместители, которые называются алкильными группами.
Имеется 3 пентана, 5 гексанов, 9 гептанов и 18 октанов. Было бы трудно присвоить уникальные индивидуальные имена, которые мы могли бы запомнить. Систематический способ именования углеводородов и других органических соединений был разработан Международным союзом теоретической и прикладной химии (IUPAC). Эти правила, используемые во всем мире, известны как Система номенклатуры IUPAC. (Некоторые названия, которые мы использовали ранее, такие как изобутан, изопентан и неопентан, не соответствуют этим правилам и называются общих имен .) Название основы (Таблица \(\PageIndex{1}\)) указывает количество атомов углерода в самой длинной непрерывной цепи (LCC). Атомы или группы, присоединенные к этой углеродной цепи, называемые заместителями , затем называются, а их положения обозначаются цифрами. Сейчас мы будем рассматривать только те заместители, которые называются алкильными группами.
| Стержень | Номер |
|---|---|
| мет- | 1 |
| эт- | 2 |
| опора- | 3 |
| а- | 4 |
| ожидание — | 5 |
| шестигранник- | 6 |
| гепт- | 7 |
| окт- | 8 |
| не | 9 |
| дек- | 10 |
Алкильная группа представляет собой группу атомов, образующуюся при удалении одного атома водорода из алкана.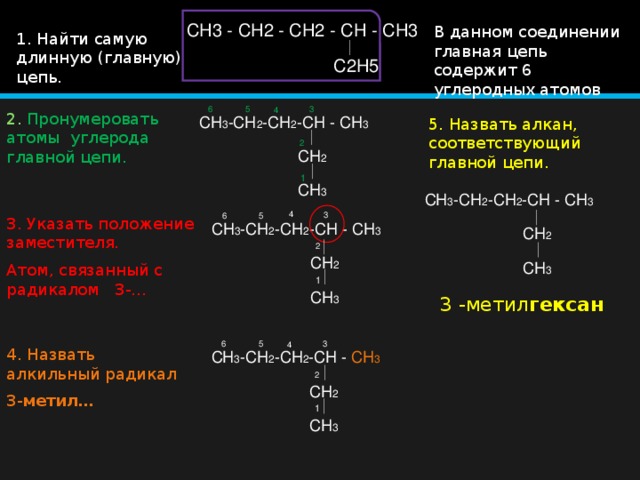 Группа названа путем замены суффикса -ane исходного углеводорода на .-ил . Например, группа -CH 3 , полученная из метана (CH 4 ), получается в результате вычитания одного атома водорода и называется метильной группой . Алкильные группы, которые мы будем использовать чаще всего, перечислены в таблице \(\PageIndex{2}\). Алкильные группы не являются независимыми молекулами; это части молекул, которые мы рассматриваем как единое целое, чтобы систематически называть соединения.
Группа названа путем замены суффикса -ane исходного углеводорода на .-ил . Например, группа -CH 3 , полученная из метана (CH 4 ), получается в результате вычитания одного атома водорода и называется метильной группой . Алкильные группы, которые мы будем использовать чаще всего, перечислены в таблице \(\PageIndex{2}\). Алкильные группы не являются независимыми молекулами; это части молекул, которые мы рассматриваем как единое целое, чтобы систематически называть соединения.
| Исходный алкан | Алкильная группа | Концентрированная структурная формула | ||
|---|---|---|---|---|
| We will introduce the other three where appropriate.»> метан | метил | СН 3 – | ||
| этан | этил | We will introduce the other three where appropriate.»> CH 3 CH 2 – | ||
| пропан | пропил | CH 3 CH 2 CH 2 – | ||
| We will introduce the other three where appropriate.»> изопропил | (CH 3 ) 2 CH– | |||
| бутан | бутил* | CH 3 CH 2 CH 2 CH 2 – | ||
* Имеется четыре бутильных группы, две из которых получены из бутана, а две — из изобутана.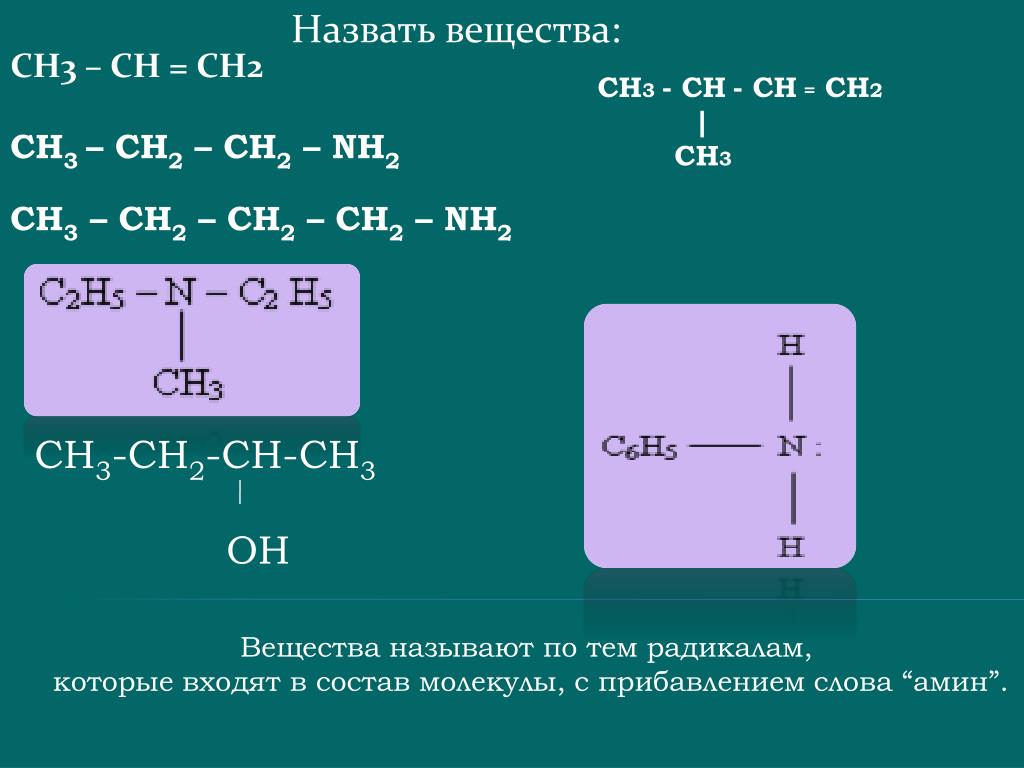 Мы представим остальные три, где это уместно. Мы представим остальные три, где это уместно. | ||||
Упрощенные правила ИЮПАК для обозначения алканов следующие (показаны в примере \(\PageIndex{1}\)).
1. Назовите алканы в соответствии с LCC (самая длинная непрерывная цепь) атомов углерода в молекуле (а не общим числом атомов углерода). Этот LCC, считающийся материнской цепью, определяет название основания, к которому мы добавляем суффикс — ан , чтобы указать, что молекула является алканом.
2. Если углеводород разветвлен, пронумеруйте атомы углерода LCC. Номера присваиваются в том направлении, которое дает наименьшие номера атомам углерода с присоединенными заместителями. Дефисы используются для отделения чисел от названий заместителей; запятые отделяют числа друг от друга. (LCC не нужно писать прямой линией; например, LCC в следующем примере имеет пять атомов углерода.)
3. Расположите названия групп заместителей в алфавитном порядке перед названием исходного соединения. Если одна и та же алкильная группа встречается более одного раза, указываются номера всех атомов углерода, к которым она присоединена. Если одна и та же группа появляется более одного раза у одного и того же атома углерода, номер этого атома углерода повторяется столько раз, сколько появляется группа. Причем количество одинаковых групп обозначается греческими префиксами di -, три -, тетра — и так далее. Эти префиксы , а не учитываются при определении алфавитного порядка заместителей. Например, этил указан перед диметилом; di- просто игнорируется. Последняя названная алкильная группа ставится перед названием исходного алкана, образуя одно слово.
Если одна и та же алкильная группа встречается более одного раза, указываются номера всех атомов углерода, к которым она присоединена. Если одна и та же группа появляется более одного раза у одного и того же атома углерода, номер этого атома углерода повторяется столько раз, сколько появляется группа. Причем количество одинаковых групп обозначается греческими префиксами di -, три -, тетра — и так далее. Эти префиксы , а не учитываются при определении алфавитного порядка заместителей. Например, этил указан перед диметилом; di- просто игнорируется. Последняя названная алкильная группа ставится перед названием исходного алкана, образуя одно слово.
При соблюдении этих правил каждое уникальное соединение получает собственное эксклюзивное имя. Правила позволяют нам не только называть соединение по заданной структуре, но и рисовать структуру по заданному имени. Лучший способ научиться пользоваться системой IUPAC — это заставить ее работать, а не просто запомнить правила. Это проще, чем кажется.
Это проще, чем кажется.
Пример \(\PageIndex{1}\)
Назовите каждое соединение.
Решение
- LCC имеет пять атомов углерода, поэтому исходным соединением является пентан (правило 1). Ко второму атому углерода пентановой цепи присоединена метильная группа (правило 2). Поэтому название 2-метилпентан.
- LCC имеет шесть атомов углерода, поэтому исходным соединением является гексан (правило 1). Метильные группы (правило 2) присоединены ко второму и пятому атомам углерода. Название 2,5-диметилгексан.
- LCC имеет восемь атомов углерода, поэтому исходным соединением является октан (правило 1). Имеются метильная и этильная группы (правило 2), обе присоединены к четвертому атому углерода (если считать от вправо, то дает этому атому углерода меньший номер; правило 3). Таким образом, правильное название – 4-этил-4-метилоктан.
Упражнение \(\PageIndex{1}\)
Назовите каждое соединение.
Пример \(\PageIndex{2}\)
Нарисуйте структуру каждого соединения.
- 2,3-диметилбутан
- 4-этил-2-метилгептан
Решение
Рисуя структуры, всегда начинайте с родительской цепочки.
- Исходной цепью является бутан, что указывает на четыре атома углерода в LCC.
Затем добавьте группы на свои места. Вы можете нумеровать родительскую цепочку в любом направлении, если вы непротиворечивы; просто не меняйте направление до того, как структура будет готова. Название указывает на два метила (CH 3 ), одна у второго атома углерода и одна у третьего.
Наконец, заполните все атомы водорода, имея в виду, что каждый атом углерода должен иметь четыре связи.
- В данном случае исходной цепью является гептан, что указывает на семь атомов углерода в LCC. –С–С–С–С–С–С–С–
Добавление групп в соответствующие позиции дает
Заполнение всех атомов водорода дает следующие сокращенные структурные формулы:
Обратите внимание, что облигации (тире) могут быть показаны или нет; иногда они необходимы для расстановки.


Всего комментариев: 0