3D биопринтинг: 3D Bioprinting Solutions — лаборатория биотехнологических исследований
Печать органов: как продвинулись технологии 3D-биопринтинга и что мешает их развитию
Rusbase
12 ноября 2019
Искусственное создание человеческой кожи, тканей и внутренних органов может восприниматься как фантастика, но большая часть всего этого происходит прямо сейчас. В исследовательских центрах и больницах по всему миру достижения в области 3D-печати и биопечати предоставляют новые возможности для лечения людей и научных исследований. В ближайшие десятилетия биопечать может стать следующей важной вехой в здравоохранении и персонализированной медицине.
Расскажем о технологии биопечати, последних достижениях отрасли и ограничениях, с которыми сталкиваются специалисты.
Как работает 3D-принтер
Традиционные принтеры, такие, как у вас дома или офисе, работают в двух измерениях. Они могут печатать текст или изображения на плоской поверхности (обычно на бумаге), используя размеры x (горизонтальный) и y (вертикальный). 3D-принтеры добавляют еще одно измерение — глубину (z). В процессе печати головки принтера могут перемещаться вверх и вниз, влево и вправо, вперед и назад, но вместо того, чтобы доставлять чернила на бумагу, распределяют различные материалы — полимеры, металл, керамику и даже шоколад — до «печати» целостного, объемного предмета, слой за слоем в процессе, известном как «аддитивное производство».
3D-принтеры добавляют еще одно измерение — глубину (z). В процессе печати головки принтера могут перемещаться вверх и вниз, влево и вправо, вперед и назад, но вместо того, чтобы доставлять чернила на бумагу, распределяют различные материалы — полимеры, металл, керамику и даже шоколад — до «печати» целостного, объемного предмета, слой за слоем в процессе, известном как «аддитивное производство».
Чтобы создать 3D-объект, нужен его план — цифровой файл, созданный с помощью программного обеспечения для моделирования. После его создания сгенерированная компьютером модель отправляется на принтер. Выбранный вами материал загружен в устройство и готов к нагреву, чтобы легко вытекать из сопла принтера. Когда принтер читает план, его головка перемещается, внося последовательные слои выбранного материала для создания конечного продукта.
Когда каждый слой печатается, он превращается в твердую форму либо путем охлаждения, либо за счёт смешивания двух разных растворов, доставляемых головкой принтера. Новые слои точно ложатся на предыдущие, чтобы получился устойчивый, связный элемент. Таким способом можно создать практически любую форму, включая движущуюся.
Новые слои точно ложатся на предыдущие, чтобы получился устойчивый, связный элемент. Таким способом можно создать практически любую форму, включая движущуюся.
3D-печать позволяет создавать объекты с геометрическими структурами, которые было бы трудно или невозможно сделать другими способами. Широкий ассортимент продуктов уже создается с использованием 3D-принтеров, включая ювелирные изделия, одежду, игрушки, высококачественные промышленные товары. Даже 10-летний московский школьник научился работать на 3D-принтере: печатает 3D-фигуры на заказ и продает их через Instagram.
Как работает биопринтер
Биопринтеры работают почти так же, как и 3D-принтеры, с одним ключевым отличием — они наносят слои биоматериала, который может включать живые клетки, для создания сложных структур, таких как кровеносные сосуды или ткани кожи.
Живые клетки? Где они их берут? Каждая ткань в организме состоит из разных типов клеток. Необходимые клетки (почек, кожи и так далее) берут у пациента и затем культивируют до тех пор, пока их не станет достаточно для создания «био-чернил», которые загружаются в принтер. Это не всегда возможно, поэтому для некоторых тканей берут стволовые клетки, которые способны становиться любой клеткой в теле (организме), или, например, свиной коллагеновый белок, морские водоросли и другие.
Это не всегда возможно, поэтому для некоторых тканей берут стволовые клетки, которые способны становиться любой клеткой в теле (организме), или, например, свиной коллагеновый белок, морские водоросли и другие.
Часто в биопечати используют хитозан — полисахарид, полученный из внешнего скелета моллюсков (например, креветок) или путем брожения грибов. Этот материал имеет высокую биосовместимость и обладает антибактериальными свойствами. Его недостаток — низкая скорость гелеобразования. Другой популярный материал — полисахарид, выделенный из морских водорослей, под названием агароза. Его преимущества — высокая стабильность и возможность нетоксичного сшивания при исследованиях. Однако этот биоматериал не разлагается и обладает плохой клеточной адгезией (способностью клеток слипаться друг с другом и с другими субстратами).
Первичный структурный белок, который содержится в коже и других соединительных тканях — коллаген — имеет высокую биологическую значимость.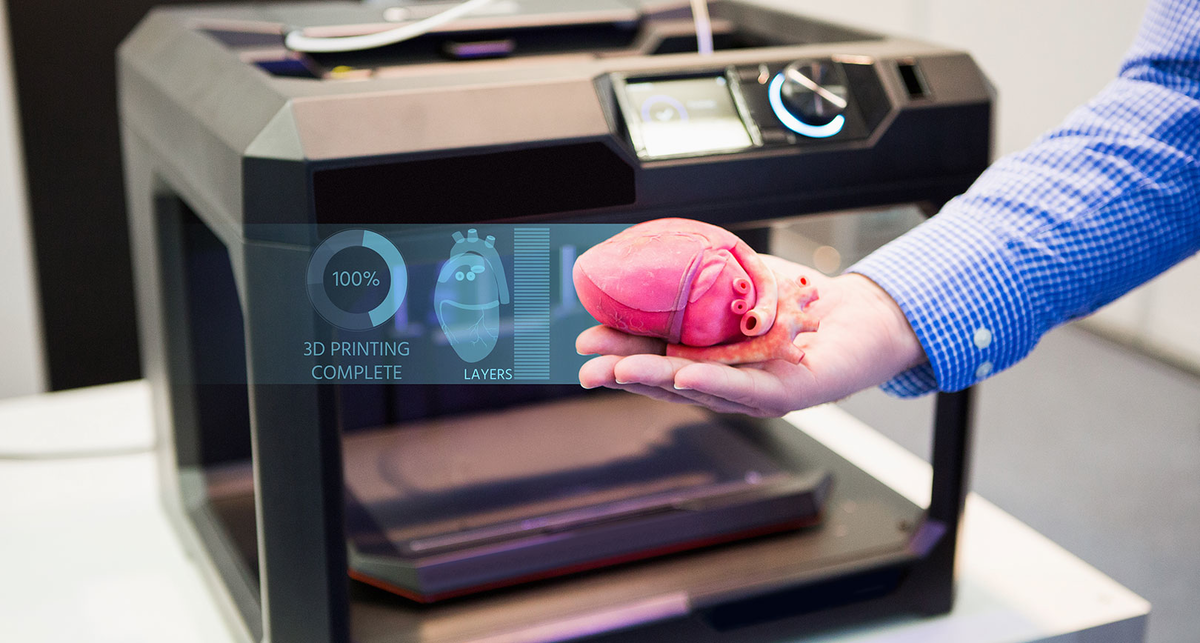 Он является наиболее распространенным белком млекопитающих и основным компонентом соединительной ткани. К его недостаткам для биопечати относят свойство кислоторастворимости. Больше информации о биоматериалах можно найти здесь.
Он является наиболее распространенным белком млекопитающих и основным компонентом соединительной ткани. К его недостаткам для биопечати относят свойство кислоторастворимости. Больше информации о биоматериалах можно найти здесь.
На основе компьютерных проектов и моделей, часто сканирований и МРТ, сделанных непосредственно у пациента, головки принтера размещают ячейки именно там, где они необходимы, и в течение нескольких часов органический объект строится из большого количества очень тонких слоев.
Биопринтер Organovo создает ткани, которые имитируют структуру и состав различных органов человека
Источник: Pbs.org
«Строительные леса» для замены ушей или носа в лаборатории Университета Уэйк Форест в Уинстон-Сейлеме, Северная Каролина
Источник: CBS News
Компьютер отображает изображение «лесов» для человеческого уха, созданного в лаборатории Университета Уэйк Форест в Уинстон-Сейлеме, Северная Каролина
Источник: CBS News
Как правило, нужно больше, чем просто клетки, поэтому большинство биопринтеров также поставляют какой-то органический или синтетический «клей» — растворимый гель или коллагеновый каркас, к которому клетки могут прикрепляться и расти. Это помогает им формироваться и стабилизироваться в правильной форме. Удивительно, но некоторые клетки могут принять правильное положение сами по себе без каких-либо «строительных лесов». Как они узнают, куда идти? А как клетки эмбриона развиваются в матке или ткань взрослого человека движется для восстановления повреждений? Так же и здесь.
Это помогает им формироваться и стабилизироваться в правильной форме. Удивительно, но некоторые клетки могут принять правильное положение сами по себе без каких-либо «строительных лесов». Как они узнают, куда идти? А как клетки эмбриона развиваются в матке или ткань взрослого человека движется для восстановления повреждений? Так же и здесь.
Университеты, исследователи и частные компании по всему миру вовлечены в развитие технологий биопечати. Давайте посмотрим на некоторые из удивительных вещей, над которыми они работают.
Биопринтинг в России
3D Bioprinting Solutions — лаборатория биотехнологических исследований, основанная медицинской компанией INVITRO. Деятельность лаборатории — разработка и производство биопринтеров и материалов в области трехмерной биопечати и научные исследования. 23 августа 2019 года лаборатория «3Д Биопринтинг Солюшенс» отправила на МКС новую партию кювет для продолжения экспериментов по биопечати в космосе, начатых в 2018 году. Об этом сообщили в пресс-центре лаборатории. На этот раз на первом в мире космическом биопринтере Organ.Aut планируется использовать органические и неорганические компоненты для сборки костной ткани.
На этот раз на первом в мире космическом биопринтере Organ.Aut планируется использовать органические и неорганические компоненты для сборки костной ткани.
Симпозиум «Биофабрикация в космосе»
Источник: Zdrav.Expert
Магнитный биопринтер Organ.Aut
Источник: Zdrav.Expert
Также космонавты будут выращивать белковые кристаллы и экспериментировать с печатью биоплёнок бактерий для изучения их поведения в условиях невесомости. Российские учёные ожидают получить уникальные научные данные, которые могут быть применимы при разработке новых лекарственных препаратов.
Научный руководитель компании «3Д Биопринтинг Солюшенс» и ведущий научный сотрудник Института регенеративной медицины, кандидат медицинских наук Владимир Миронов в своем выступлении на кафедре анатомии Сеченовского Университета 2 сентября отметил: «Живые клетки, ткани и органы человека будут синтезированы уже в текущем столетии. Для этого морфологические науки, такие как микроскопическая анатомия и гистология, надо оцифровизировать или диджитализировать, то есть перевести в цифровой формат и сделать доступными для компьютерных программ роботических биопринтеров, так как без цифровых моделей нельзя напечатать человеческие ткани и органы».
Биопринтинг в мире
Ежегодно миллионы людей во всем мире нуждаются в пересадке кости. Современные костные трансплантаты часто используют синтетический материал на основе цемента в сочетании с собственной костью пациента. Однако применение этих материалов имеет ряд ограничений — некоторые трансплантаты вызывали отторжение и воспалительные процессы у пациентов. Воспроизведение естественного «интерфейса» кость-хрящ также было проблематичным.
Тем не менее, команда из Университета Суонси в 2014 году разработала технологию биопечати, которая позволяет создать искусственный костный протез в точной форме требуемой кости, используя биосовместимый материал, который является одновременно долговечным и регенеративным. Над аналогичными исследованиями в то же время работали и ученые из Ноттингемского университета в Англии.
Чтобы напечатать небольшую кость, требуется около двух часов. Поэтому хирурги могут сделать её прямо в операционной. Затем эта часть кости покрывается стволовыми клетками взрослого человека, способными развиваться практически в любой другой тип клеток. Это сочетается с био-чернилами из принтера — комбинацией полимолочной кислоты (которая обеспечивает механическую прочность кости) и альгината — гелеобразного вещества, которое служит амортизирующим материалом для клеток. Затем конечный продукт имплантируется в организм, где в течение примерно трех месяцев полностью исчезнет и будет заменен новой костью.
Затем эта часть кости покрывается стволовыми клетками взрослого человека, способными развиваться практически в любой другой тип клеток. Это сочетается с био-чернилами из принтера — комбинацией полимолочной кислоты (которая обеспечивает механическую прочность кости) и альгината — гелеобразного вещества, которое служит амортизирующим материалом для клеток. Затем конечный продукт имплантируется в организм, где в течение примерно трех месяцев полностью исчезнет и будет заменен новой костью.
Исследователи надеются, что в будущем биопечатаемые кости могут быть созданы с достаточной надежностью, чтобы поддержать сложную реконструкцию позвоночника, и что костный материал будет дополнительно улучшен для повышения его совместимости с клетками хряща.
Источник: ETH Zurich
Успешные опыты 3D-печати человеческого хряща в скором времени могут полностью заменить искусственные имплантаты людям, нуждающимся в реконструктивной хирургии. Еще в 2015 году ученые в Цюрихе разработали технологию, которая позволит больницам печатать полноразмерный имплантат человеческого носа менее чем за 20 минут. Они считают, что любой хрящевой имплантат может быть изготовлен по их методике.
Они считают, что любой хрящевой имплантат может быть изготовлен по их методике.
Исследователь Матти Кести описал технологию так:
“
«Серьезная автомобильная авария может привести к тому, что водитель или пассажир получат сложные травмы носа. Нос можно восстановить, создав 3D-модель на компьютере. В то же время выполняется биопсия пациента, и клетки хряща удаляются из тела пострадавшего, например, из колена, пальца, уха или осколков разбитого носа. Клетки нерестятся в лаборатории и смешиваются с биополимером. Из этой суспензии с помощью биопринтера создается модель хряща носа, которая имплантируется пациенту во время операции. В процессе биополимер используется просто как форма. Впоследствии он расщепляется собственными хрящевыми клетками организма. И через пару месяцев невозможно будет различить трансплантат и собственный носовой хрящ человека».
Матти Кести
Поскольку имплантат был выращен из собственных клеток организма, риск отторжения будет гораздо ниже, чем для имплантата, сделанного, скажем, из силикона. Дополнительное преимущество заключается в том, что биоимплантат растет вместе с пациентом, что особенно важно для детей и молодых людей.
Дополнительное преимущество заключается в том, что биоимплантат растет вместе с пациентом, что особенно важно для детей и молодых людей.
Если человек сильно обожжен, здоровую кожу можно взять из другой части тела и использовать для покрытия пораженного участка. Иногда неповрежденной кожи не хватает.
Исследователи, работающие в Медицинской школе Уэйк Форест, успешно разработали, построили и протестировали принтер, который может печатать клетки кожи непосредственно на ожоговой ране. Сканер очень точно определяет размер и глубину повреждений. Эта информация передается на принтер, и печатается кожа для покрытия раны. В отличие от традиционных кожных трансплантатов, требуется только участок кожи, размер которого составляет одну десятую от размера ожога, чтобы вырастить достаточное количество клеток для печати. Пока эта технология находится на экспериментальной стадии, и исследователи надеются, что она будет широко доступна в течение следующих пяти лет.
Как уже упоминалось, 3D-принтеры печатают изделия послойно, и поскольку кожа представляет собой многослойный орган с различными типами клеток, она хорошо подходит для данного типа технологий. Тем не менее, исследователям предстоит решить еще много задач, в частности, как предотвратить повреждение клеток от тепла, выделяемого принтером. И конечно же, как и большинство частей человеческого тела, кожа более сложная, чем кажется на первый взгляд — есть нервные окончания, кровеносные сосуды и множество других аспектов, которые необходимо учитывать.
Кровеносные сосуды
Инженер-биомеханик Моника Мойя держит чашку Петри с печатными биотрубками на основе альгината. Биотрубки могут действовать как временные кровеносные сосуды, аналогичные кровеносным сосудам, которые помогают создать участок живой ткани.
Источник:embodi3D
Учитывая, что в теле человека десятки тысяч километров вен, артерий и капилляров, исследователи работают над тем, чтобы заменить их, если они когда-нибудь износятся. Создание жизнеспособных кровеносных сосудов также важно для правильной работы всех других потенциальных биопечатных частей тела.
Создание жизнеспособных кровеносных сосудов также важно для правильной работы всех других потенциальных биопечатных частей тела.
Инженер-биомеханик Моника Мойя из Ливерморской национальной лаборатории им. Лоуренса использует биопечать для создания кровеносных сосудов. Материалы, созданные ее биопринтерами, спроектированы таким образом, чтобы позволить маленьким кровеносным сосудам развиваться самостоятельно.
Эта разработка требует времени, поэтому распечатываются пробирки с клетками и другими биоматериалами, чтобы помочь доставить жизненно важные питательные вещества в окружающую печатную среду. Через некоторое время самосборные капилляры соединяются с биопечатными трубками и начинают самостоятельно доставлять питательные вещества в клетки, имитируя работу этих структур в организме человека.
Внутренние органы
Многие исследователи надеются, что через 20 лет списки пациентов, ожидающих пересадки органов, уйдут в прошлое. Они представляют мир, в котором любой орган может быть напечатан и пересажен всего за несколько часов, без отторжения и осложнений, потому что эти органы будут созданы из клеток тела в соответствии с индивидуальными особенностями каждого пациента.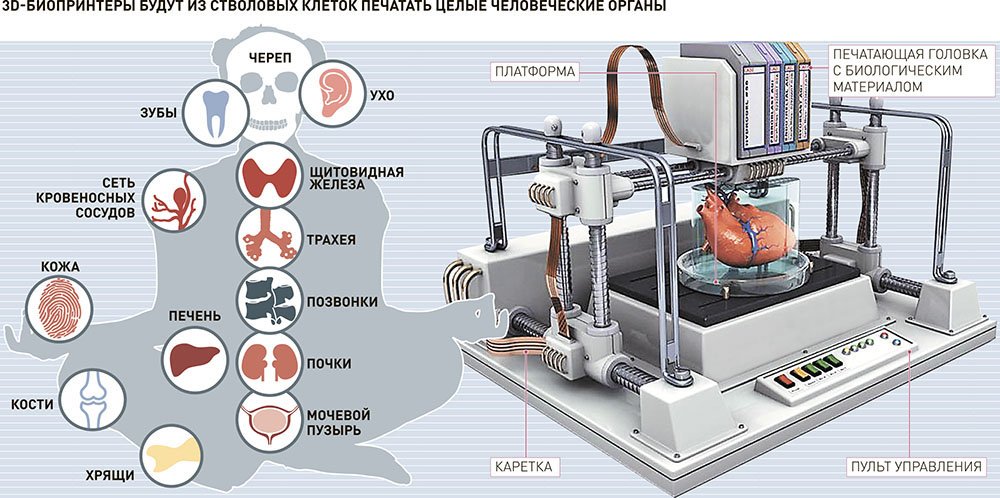 В настоящее время биопечать полностью функциональных сложных внутренних органов невозможна, но исследования постоянно ведутся (и не без успеха).
В настоящее время биопечать полностью функциональных сложных внутренних органов невозможна, но исследования постоянно ведутся (и не без успеха).
Мочевой пузырь
Например, мочевой пузырь уже печатают. В 2013 году в Университете Уэйк Форест в США исследователи успешно взяли клетки из исходного, плохо функционирующего мочевого пузыря пациента, культивировали их и добавили дополнительные питательные вещества. Затем была напечатана трехмерная форма мочевого пузыря пациента и пропитанные через нее культивируемые клетки. Форма была помещена в инкубатор и, когда она достигла нужной кондиции, её пересадили в тело пациента. Форма со временем разрушится, оставив только органический материал. Та же команда успешно создала жизнеспособные уретры.
Врачи и ученые Института регенеративной медицины Уэйк Форест (WFIRM) были первыми в мире, кто создал органы и ткани, выращенные в лабораторных условиях, которые были успешно пересажены в человека. Прямо сейчас они работают над выращиванием тканей и органов для более чем 30 различных областей тела, от почек и трахеи до хрящей и легких. Также они стремятся ускорить доступность этих методов лечения для пациентов.
Также они стремятся ускорить доступность этих методов лечения для пациентов.
Ученые в Австралии тоже занимаются подобными исследованиями. Они использовали человеческие стволовые клетки для выращивания почечного органа, который содержит все необходимые типы клеток для почек. Такие клетки могут служить ценным исходным источником для биопечати более сложной структуры почек.
Доктор медицины, профессор урологии, профессор Института регенеративной медицины Энтони Атала показывает почку, созданную биопринтером. Модифицированный настольный струйный принтер распыляет клетки вместо чернил. Клетки культивировали у пациента, а структурный шаблон для почки получили из МРТ (поэтому он имеет правильный размер и форму).
Используя эту технологию, еще в 2001 году Атала напечатал и успешно пересадил мочевой пузырь для молодого человека Джейка.
Источник: TedEd
Сердце
Клетки сердца, органоиды, выращенные в лаборатории. Источник
Удивительно, но именно сердце человека может стать одним из самых легких органов для печати, поскольку оно, по сути, представляет собой насос с трубками.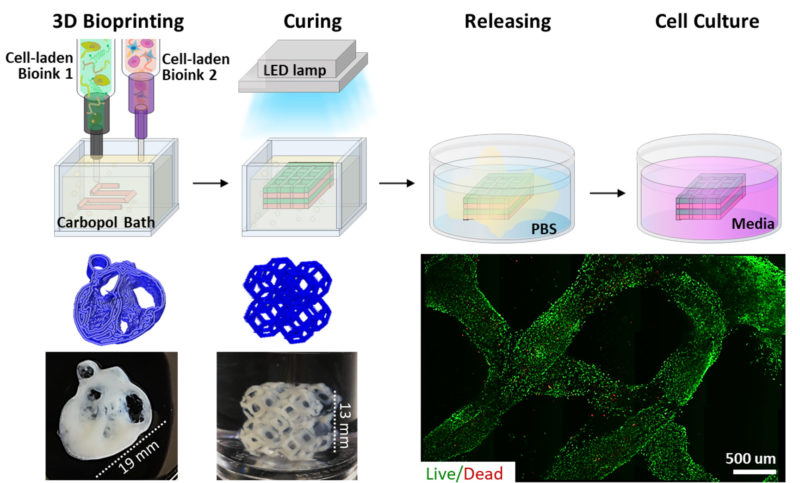 Конечно, всё не так просто, но многие исследователи считают, что человечество научится печатать сердца раньше, чем почки или печень.
Конечно, всё не так просто, но многие исследователи считают, что человечество научится печатать сердца раньше, чем почки или печень.
Исследователи Института регенеративной медицины Уэйк Форест в апреле 2015 года создали «органоиды» — напечатанные на 3D-принтере полностью функциональные, бьющиеся сердечные клетки.
В апреле 2019 года израильские ученые напечатали первое в мире трехмерное сердце. Оно еще очень маленькое, размером с вишню, но способно выполнять свои функции. Трехмерное сердце с кровеносными сосудами использует персонализированные «чернила» из коллагена, белка, который поддерживает клеточные структуры, и других биологических молекул.
Исследователь из Тель-Авивского университета держит первое в мире трехмерное печатное сердце, 15 апреля 2019 года.
Источник: Haaretz
«Это первый случай, когда кто-либо где-либо успешно спроектировал и напечатал целое сердце с клетками, кровеносными сосудами, желудочками и камерами», — рассказал ученый Тель-Авивского университета профессор Тал Двир.
До сих пор ученым удавалось печатать ткани хряща и, например, аортального клапана, но задача заключалась в том, чтобы создать ткани с васкуляризацией — кровеносными сосудами, включая капилляры, без которых органы не могут выжить, не говоря уже о функционировании.
Тель-авивские ученые начали с жировой людской ткани и разделили клеточные и неклеточные компоненты. Затем они перепрограммировали клетки, чтобы те превратились в недифференцированные стволовые клетки, которые затем могли бы стать сердечными или эндотелиальными. Эндотелий — однослойный пласт плоских клеток, выстилающий внутреннюю поверхность сердечных полостей, кровеносных и лимфатических сосудов. Клетки эндотелия исполняют множество функций сосудистой системы, например, контролируют артериальное давление, регулируют компоненты свертывания крови и формирование новых кровеносных сосудов.
Неклеточные материалы, включая большое количество белков, были переработаны в «персонализированный гидрогель», который служил «чернилами для печати».
Пройдут годы, прежде чем эта технология сможет создавать органы для эффективной трансплантации. Тем не менее, достижения ученых в Тель-Авиве являются огромной вехой на этом пути.
Медицинские исследования и фармакология
Одна из ключевых потенциальных областей использования биопечатных живых материалов — это область медицинских испытаний и исследований лекарственных препаратов. Биопечатные ткани обладают несколькими типами клеток с разной плотностью и ключевыми архитектурными особенностями. Благодаря этому исследователи могут изучать воздействие различных заболеваний на организм, этапы прогрессирования заболевания и возможные способы лечения в естественной микросреде.
Одним из самых впечатляющих достижений последних лет является разработка «настольного мозга» в Центре передовых технологий ARC в 2016 году. Исследователи смогли с помощью 3D-принтера создать трехмерную печатную шестислойную структуру, включающую нервные клетки, которые имитируют структуру мозговой ткани.
Это открывает огромные потенциальные выгоды для исследователей, фармацевтических и частных компаний, потому что позволит им тестировать новые продукты и лекарства на ткани, которая точно отражает реакции ткани человеческого мозга, в отличие от образцов животных, которые могут вызывать совершенно другую реакцию. «Настольный мозг» также может быть использован для дальнейшего исследования таких заболеваний, как шизофрения или болезнь Альцгеймера.
Мы еще далеки от печати мозга, но способность располагать клетки так, чтобы они образовывали нейронные сети, является значительным шагом вперед. Позволяя исследователям работать с человеческими тканями в режиме реального времени, можно значительно ускорить процессы тестирования и давать более реалистичные и точные результаты. Это также снизит необходимость использования лабораторных животных для медицинских анализов и потенциально опасных испытаний на людях.
Медицинские тренажеры и реестры данных
Источник: Simbionix
В настоящее время в мире используется около 3000 медицинских тренажеров, помогающих врачам практиковаться в выполнении сложных процедур. Виртуальные кровеносные сосуды, 3D-печатные органы… и ни одно животное не страдает!
Виртуальные кровеносные сосуды, 3D-печатные органы… и ни одно животное не страдает!
Американская компания 3D Systems создала отраслевой сегмент под названием VSP (Virtual Surgical Planning). Этот подход к персонализированной хирургии сочетает в себе знания в области медицинской визуализации, хирургического моделирования и 3D-печати. Хирурги, впервые использующие медицинский симулятор Simbionix, часто сообщают о чувстве физической боли, сопереживая своему виртуальному пациенту — опыт настолько реалистичен. Органы и ткани выглядят совершенно реальными. При сшивании органа хирург видит на экране иглу, попадающую в ткань, и натягивает нить. Если врач делает что-то не так, виртуальные кровеносные сосуды ломаются, и орган начинает кровоточить. Эти симуляторы были разработаны израильской компанией «Симбионикс», которую в 2014 году выкупила 3D Systems.
3 сентября 2019 года Общество радиологии Северной Америки (RSNA) и Американский колледж радиологии (ACR) объявили о запуске нового реестра клинических данных медицинской 3D-печати, чтобы собирать сведения о результатах лечения с использованием 3D-печати по месту оказания медицинской помощи. Эта информация станет мощным инструментом для оценки и улучшения качества обслуживания пациентов в режиме реального времени, будет стимулировать текущие исследования и разработки, информировать пациентов и медицинских работников о наилучшем курсе лечения.
Эта информация станет мощным инструментом для оценки и улучшения качества обслуживания пациентов в режиме реального времени, будет стимулировать текущие исследования и разработки, информировать пациентов и медицинских работников о наилучшем курсе лечения.
“
«Создание объединенного реестра 3D-печати RSNA-ACR имеет важное значение для развития клинической 3D-печати. Реестр позволит собирать данные в поддержку надлежащего использования этой технологии и ее значения для принятия клинических решений».
Уильям Уидок, профессор радиологии в Университете Мичигана и председатель RSNA 3D Printing Special Interest Group (SIG)
По данным RSNA, сведения в реестре позволят провести необходимый анализ, чтобы продемонстрировать клиническую ценность 3D-печати. Из-за большого разнообразия клинических показаний, различных технологий для создания физических моделей из медицинских изображений и сложности моделей проблематично выбрать оптимальный метод лечения. Реестр поможет решить эту проблему.
Программное обеспечение для биопечати
Производитель биопринтеров и программного обеспечения для биопечати Allevi 5 сентября 2019 года представил программное обеспечение Allevi Bioprint Pro. Встроенная генерация моделей и интегрированная нарезка позволит больше сосредоточиться на проведении экспериментов, а не на настройке принтера. Программа работает полностью в облаке, а это означает, что можно создавать свои биоструктуры, определять материалы и отслеживать отпечатки прямо из веб-браузера на любом компьютере.
По словам команды разработчиков, новый биопринтер с вышеуказанным ПО мощный и простой в использовании и представляет собой еще один кусочек головоломки на пути к печати органов с помощью 3D-принтера.
В то же время первая компания в сегменте bio-ink CELLINK объявила о выпуске нового продукта, призванного стать самой гибкой платформой для биопечати на рынке. В не имеющем на данный момент аналогов биопринтере BIO X6 реализована возможность объединения большего количества материалов для биопечати, ячеек и инструментов.
Почему всё это так долго?
Сложная структура тела
Тело человека и его различные компоненты намного сложнее пластиковой игрушки. Человеческий орган имеет сложную сеть клеток, тканей, нервов и структур, которые должны быть расположены определенным образом для правильного функционирования. От размещения тысяч крошечных капилляров в печени до фактического получения напечатанного сердца, которое «бьётся» и сжимается в людском теле — еще много исследований и испытаний.
Правовое регулирование
Кроме того, биопечатные технологии, как и все новые медицинские методы лечения, должны пройти тесты безопасности и надлежащие процессы правового регулирования, прежде чем станут доступны.
Специальное программное и аппаратное обеспечение
Также необходимо время для разработки специального программного и аппаратного обеспечения. Написать эти программы можно лишь имея соответствующие данные (медицинские, клинические, статистические, математические и так далее), которые кто-то должен предварительно собрать, проанализировать, систематизировать и перевести в цифровую форму.
Работа над всеми этими этапами требует интеграции технологий из различных областей, включая инженерию, науку о биоматериалах, клеточную биологию, физику, математику и медицину. Так что нам нужно быть немного более терпеливыми.
Главное — знать, что те, кто работает на местах, врачи и инженеры, программисты и ученые каждый день делают успехи как в самой технологии биопечати, так и в понимании того, как ее можно использовать и совершенствовать. Хотя мы еще не совсем там, нет сомнений, что лет через 10-20 медицина будет совсем другой в том числе благодаря биопечати.
Коротко о главном
Биопечать – это расширение традиционной 3D-печати.
Биопринтинг может производить живые ткани, кости, кровеносные сосуды и, возможно, целые органы для использования в медицинских процедурах, тренировках медперсонала и тестировании.
Клеточная сложность живого организма привела к тому, что 3D-биопечать развивается медленнее, чем обычная 3D-печать..jpg)
Технология биопечати может дать возможность генерировать ткани, специфичные для пациента, для разработки точных, целенаправленных и полностью персонализированных процедур.
Нам еще предстоит пройти долгий путь, прежде чем мы сможем создать полностью функционирующие и жизнеспособные органы для трансплантации человеку.
Материалы по теме:Россия первой в мире напечатала живые ткани в космосе с помощью биопринтера
5 самых удивительных вещей, созданных с помощью 3D-печати
В 2021 году на орбиту отправится ракета, напечатанная на 3D-принтере
«Экспонаты трогать разрешается»: как 3D-печать трансформирует музеи
© Rusbase, 2019
Автор: Надежда Алейник
Фото на обложке: etonastenka, Depositphotos
3D-биопринтинг – как создать трансплантабельный орган?
Эксперт научно-исследовательской лаборатории ДГТУ «Инженерные технологии в медицине» Сергей Чапек о том, как можно производить живые ткани из гидрогеля.
– Что такое 3D-биопринтинг?
– 3D-биопринтинг – это технология создания объёмных моделей на клеточной основе с использованием 3D-печати. Технология состоит в том, что вместо привычного для принтинга пластика мы используем гидрогель и живые клетки для создания трехмерной структуры (скаффолда). Гидрогель – это искусственный влагопоглощающий материал на основе гидрофильных природных полимеров, который способствует накоплению и сохранению влаги. Этот гидрогель используется в качестве биочернил, непосредственно того сырья, из которого получается конечный продукт.
– Для чего нужен 3D-биопринтинг?
– Это одна из самых перспективных технологий для выращивания и производства тканей и в перспективе – человеческих органов. Производство трансплантабельного органа – одна из важнейших задач, которая стоит сейчас перед наукой. Миллионы людей страдают от травм или повреждений тканей и органов, таких как повреждения периферических нервов и сердечные приступы.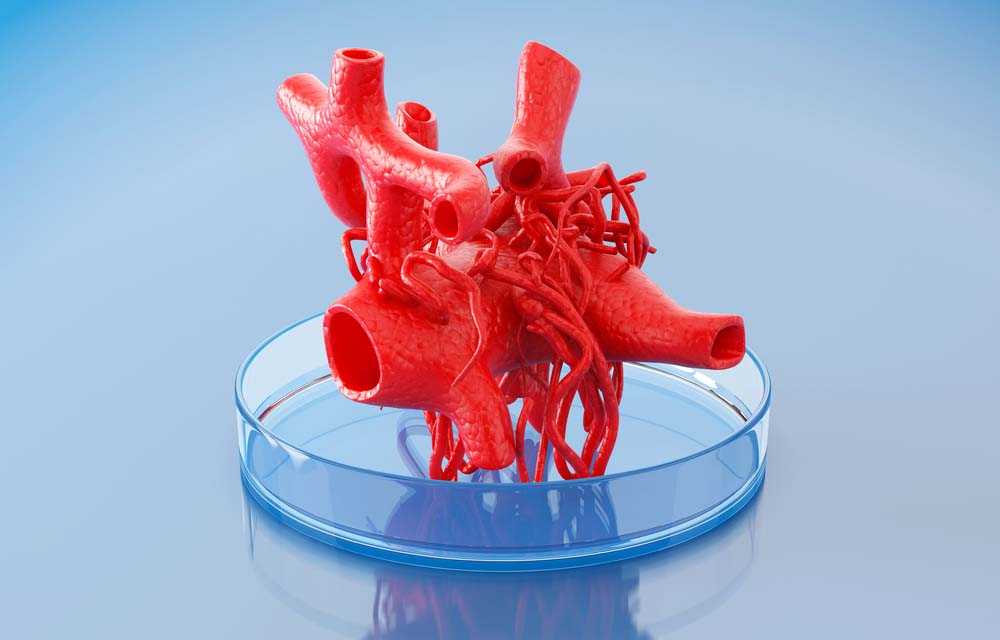 Но, к сожалению, доступность органов для трансплантации очень сильно ограничена. Для решения этой проблемы тканевая инженерия нацелена на производство заменителей тканей и органов для улучшения существующих подходов к лечению. Успехи в тканевой инженерии означали бы, что любой человек, у которого есть травма тканей или органов, может пойти в больницу, имплантировать инженерный заменитель в свое тело и тем самым полностью восстановить функцию здорового тела. Конечно, выращивание полноценного органа человека или животного, на мой взгляд, станет возможно очень нескоро. Однако в этой среде уже есть колоссальный прорыв – создание микроткани для индивидуального подбора лекарственной терапии во время лечения онкозаболеваний. Мы говорим о лечении сложных заболеваний, которые требуют изучения и подбора лекарственной терапии.
Но, к сожалению, доступность органов для трансплантации очень сильно ограничена. Для решения этой проблемы тканевая инженерия нацелена на производство заменителей тканей и органов для улучшения существующих подходов к лечению. Успехи в тканевой инженерии означали бы, что любой человек, у которого есть травма тканей или органов, может пойти в больницу, имплантировать инженерный заменитель в свое тело и тем самым полностью восстановить функцию здорового тела. Конечно, выращивание полноценного органа человека или животного, на мой взгляд, станет возможно очень нескоро. Однако в этой среде уже есть колоссальный прорыв – создание микроткани для индивидуального подбора лекарственной терапии во время лечения онкозаболеваний. Мы говорим о лечении сложных заболеваний, которые требуют изучения и подбора лекарственной терапии.
– Получается, что биопринтинг – это некий стык разных дисциплин?
– Именно. Биопринтинг – яркий пример междисциплинарного подхода к решению сложных задач. В нём сочетаются химия, физика, биология и технические науки, это некая конвергенция науки и технологий. Чтобы получить готовый продукт, нужно понимать его физические и биомеханические свойства. Думаю, что в перспективе появится профессия, «инженер в области биологической печати», которая станет логическим развитием направления тканевой инженерии. Это будут междисциплинарные профессионалы с бэкграундом из самых разных научных отраслей.
В нём сочетаются химия, физика, биология и технические науки, это некая конвергенция науки и технологий. Чтобы получить готовый продукт, нужно понимать его физические и биомеханические свойства. Думаю, что в перспективе появится профессия, «инженер в области биологической печати», которая станет логическим развитием направления тканевой инженерии. Это будут междисциплинарные профессионалы с бэкграундом из самых разных научных отраслей.
– Как осуществляется 3D-биопринтинг?
– Процесс можно разделить на 3 основных этапа: пре-биопринтинг, биопринтинг, пост-биопринтинг. Первый этап – подготовительный, составление модели для печати. Например, наша задача – напечатать трехмерный орган. Мы берем снимки компьютерной томографии и составляем из них 3D-модель. Второй этап – непосредственный принтинг с помощью биочернил: мы загружаем модель в программу для печати и получаем конструкт, состоящий из гидрогеля и живых клеток. Сам этот процесс очень быстрый, занимает максимум несколько десятков минут, в зависимости от сложности модели. Третий, пост-биопринтинг – мы берем конструкт и помещаем его в CO2-инкубатор, где созданы условия, как в живом организме, то есть температура 37 градусов и 5 процентов углекислого газа. Клетки начинают расти, и на выходе мы получаем, к примеру, микроткань.
Третий, пост-биопринтинг – мы берем конструкт и помещаем его в CO2-инкубатор, где созданы условия, как в живом организме, то есть температура 37 градусов и 5 процентов углекислого газа. Клетки начинают расти, и на выходе мы получаем, к примеру, микроткань.
– Возможно ли использовать 3D-биопринтинг в других областях, кроме медицины?
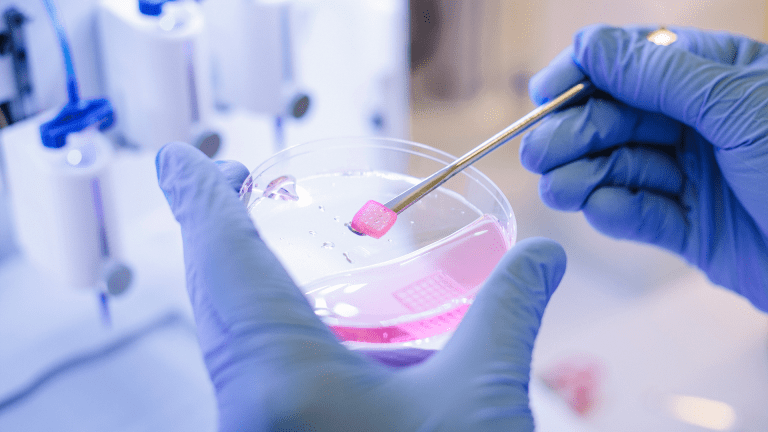
– Да, безусловно. Мы сейчас активно работаем над тем, чтобы расширить горизонты 3D-биопринтинга. Относительно недавно в мире появилось такое понятие, как green bioprinting, зеленая биопечать, в которой в качестве живых клеток в биочернилах используют не клетки животных и человека, а клетки растений. Мы уже провели несколько успешных экспериментов, используя в качестве модельного организма всем известную одноклеточную зеленую водоросль хлореллу (прим. — фото 2,3). Для чего нам это нужно? Первое – хлореллу можно использовать в агропромышленном комплексе для проращивания растений. Второе – хлореллу активно используют с середины 20-го века в качестве генератора кислорода в закрытых экосистемах. На сегодняшний день есть ряд научных публикаций, показывающих возможность применения хлореллы в качестве сателлита кислорода для работы с клетками животных.
На сегодняшний день есть ряд научных публикаций, показывающих возможность применения хлореллы в качестве сателлита кислорода для работы с клетками животных.
– Как лично Вы пришли к 3D-биопринтингу?
– С 2016 года я активно занимаюсь аддитивными технологиями, а биопечать – это один из видов таких технологий, при которых мы добавляем материал, а не вычитаем, как при традиционных видах производства (фрезеровка и т. д.). Уже в 2016 году я пришел к выводу: чтобы добиться качественных результатов, нужно выходить из зоны комфорта. Моей зоной комфорта были исключительно инженерные технологии. Поэтому я решил соединить инженерные технологии, тот бэкграунд, который у меня уже был, с биологией и химией. Результатом стали разработанные в прошлом году принтеры для научных целей. Уже в 2019 году мы побывали на научной конференции по 3D-биопринтингу в городе Нанте (прим. — Франция), на которой представили модель бюджетного биопринтера. Стоимость производства такого принтера – в пределах 150 долларов, тогда как самый дешёвый коммерческий принтер стоит несколько тысяч.
– Что сейчас происходит в сфере 3D-биопринтинга в России и в мире?
– Отрасль новая, и в мире на сегодняшний день порядка 10 активных компаний, которые производят полноценные установки для 3D-биопринтинга. Зарегистрировано чуть больше 100 компаний и предпринимателей, занимающихся 3D-биопринтингом. Для мирового рынка это очень мало. Рынок довольно сложный: мало научиться печатать какие-либо конструкты, нужно понимать, какова их дальнейшая судьба, где это будет использовано. В России есть только одна компания, которая активно занимается биопринтингом — 3D Bioprinting Solutions. Это отцы-основатели российской биопечати, которые очень много сделали для 3D-биопринтинга и продолжают её развивать у нас в стране. ДГТУ сегодня ведет очень активную деятельность в этом направлении. У нас планируется много интересных проектов.
3D-биопечать живых тканей
Прогресс в тестировании лекарств и регенеративной медицине мог бы значительно выиграть от лабораторно-инженерных тканей человека, построенных из различных типов клеток с точной трехмерной архитектурой. Но производство человеческих тканей размером более миллиметра было ограничено из-за отсутствия методов создания тканей со встроенными поддерживающими жизнь сосудистыми сетями.
Но производство человеческих тканей размером более миллиметра было ограничено из-за отсутствия методов создания тканей со встроенными поддерживающими жизнь сосудистыми сетями.
Воспроизвести
В этом видео команда Института Висса и Гарвардского университета SEAS использует настраиваемый метод 3D-биопечати для создания толстой васкуляризированной тканевой структуры, состоящей из стволовых клеток человека, коллективного матрикса и эндотелиальных клеток кровеносных сосудов. Их работа закладывает основу для продвижения методов замещения тканей и тканевой инженерии. Предоставлено: Лаборатория Льюиса, Институт Висса Гарвардского университета
Междисциплинарные исследования в Институте Висса привели к разработке метода 3D-биопечати из нескольких материалов, который позволяет создавать васкуляризированные ткани, состоящие из живых клеток человека, которые почти в десять раз толще, чем ткани, сконструированные ранее, и которые могут поддерживать свою архитектуру и функции в течение более длительного времени.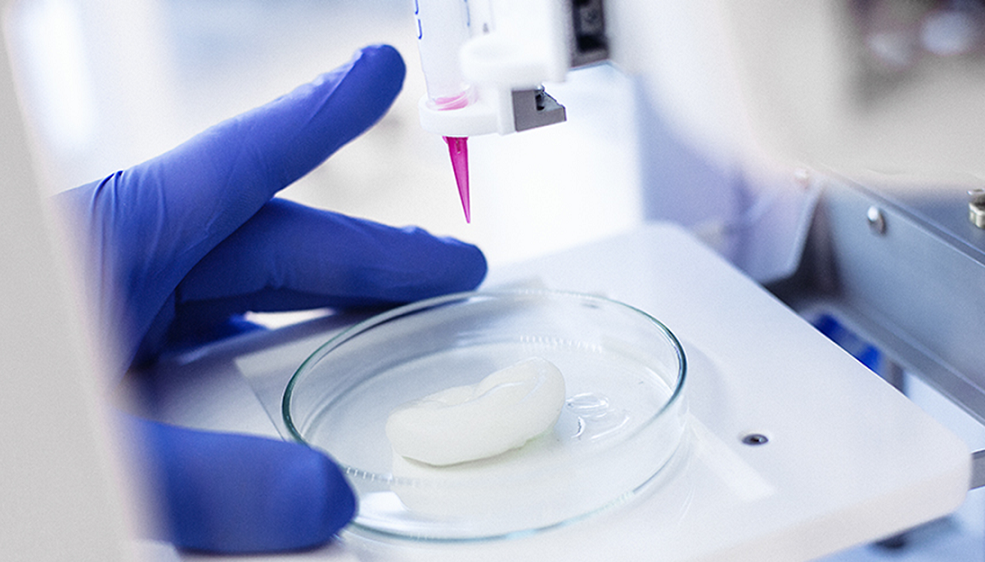 из шести недель. В этом методе используется настраиваемая силиконовая форма с печатным рисунком для размещения и размещения печатной ткани на чипе. Внутри этой формы печатается сетка более крупных сосудистых каналов, содержащих живые эндотелиальные клетки в силиконовых чернилах, в которую в отдельном задании на печать наслаиваются самоподдерживающиеся чернила, содержащие живые мезенхимальные стволовые клетки (МСК). После печати жидкость, состоящая из фибробластов и внеклеточного матрикса, используется для заполнения открытых областей внутри конструкции, добавляя компонент соединительной ткани, который сшивает и дополнительно стабилизирует всю структуру.
из шести недель. В этом методе используется настраиваемая силиконовая форма с печатным рисунком для размещения и размещения печатной ткани на чипе. Внутри этой формы печатается сетка более крупных сосудистых каналов, содержащих живые эндотелиальные клетки в силиконовых чернилах, в которую в отдельном задании на печать наслаиваются самоподдерживающиеся чернила, содержащие живые мезенхимальные стволовые клетки (МСК). После печати жидкость, состоящая из фибробластов и внеклеточного матрикса, используется для заполнения открытых областей внутри конструкции, добавляя компонент соединительной ткани, который сшивает и дополнительно стабилизирует всю структуру.
Изображение конфокальной микроскопии, показывающее поперечное сечение напечатанной на 3D-принтере конструкции васкуляризированной ткани толщиной 1 сантиметр, показывающей дифференцировку стволовых клеток в направлении развития костных клеток после одного месяца активной перфузии жидкостей, питательных веществ и факторов роста клеток. Структура была изготовлена с использованием новой стратегии 3D-биопечати, изобретенной Дженнифер Льюис и ее командой в Институте Висса и Гарвардском университете SEAS. Предоставлено: Лаборатория Льюиса, Институт Висса при Гарвардском университете,
Структура была изготовлена с использованием новой стратегии 3D-биопечати, изобретенной Дженнифер Льюис и ее командой в Институте Висса и Гарвардском университете SEAS. Предоставлено: Лаборатория Льюиса, Институт Висса при Гарвардском университете,
. Полученная структура мягких тканей может быть немедленно перфузирована питательными веществами, а также факторами роста и дифференцировки через один вход и выход на противоположных концах чипа, которые соединяются с сосудистым каналом для обеспечения выживания. и созревание клеток. В экспериментальном исследовании биопринтированные тканевые конструкции толщиной один сантиметр, содержащие МСК костного мозга человека, окруженные соединительной тканью и поддерживаемые искусственной сосудистой оболочкой, выстланной эндотелием, обеспечивают циркуляцию факторов роста костей и, следовательно, индукцию развития костей. .
Этот инновационный подход к биопечати можно модифицировать для создания различных васкуляризированных трехмерных тканей для регенеративной медицины и тестирования лекарств. Команда Wyss также изучает возможность использования 3D-биопечати для изготовления новых версий устройств Института органов на чипах, что делает их производственный процесс более автоматизированным и позволяет разрабатывать все более сложные микрофизиологические устройства. Результатом этих усилий стал первый полностью напечатанный на 3D-принтере орган на чипе — сердце на чипе — со встроенными мягкими датчиками деформации.
Команда Wyss также изучает возможность использования 3D-биопечати для изготовления новых версий устройств Института органов на чипах, что делает их производственный процесс более автоматизированным и позволяет разрабатывать все более сложные микрофизиологические устройства. Результатом этих усилий стал первый полностью напечатанный на 3D-принтере орган на чипе — сердце на чипе — со встроенными мягкими датчиками деформации.
- 1/7 Поперечное сечение долговременной перфузии сосудистой сети, покрытой HUVEC (красного цвета), поддерживающей HNDFladen
(зеленая) матрица. - 2/7 Вид сверху вниз на долговременную перфузию сосудистой сети, покрытой HUVEC (красный цвет), поддерживающей матрикс HNDFladen (зеленый цвет).
- 3/7 Фотография поперечного сечения печатной ткани, помещенной в перфузионную камеру.
- 4/7 Фотография поперечного сечения печатной ткани, помещенной в перфузионную камеру.
- 5/7 Фотография печатной тканевой конструкции, помещенной в перфузионную камеру.

- 6/7 Фотография сосудистой сети и клеточных чернил.
- 7/7 Фотография напечатанной на 3D-принтере сосудистой сети (красная) внутри Red is the
- Следующая
- Предыдущая
Что такое 3D-биопринтинг? | Объяснение биопечати
«Трехмерная биопечать» или «биопечать» — это форма аддитивного производства, в которой вместо традиционных металлов и пластиков используются клетки и биоматериалы для создания трехмерных конструкций, представляющих собой функциональные трехмерные ткани. Эти биоматериалы называются биочернилами, и они имитируют состав наших тканей. Биопечать может применяться в различных областях, включая, помимо прочего, регенеративную медицину, открытие и разработку лекарств, а также трехмерное культивирование клеток.
3D-конструкция, напечатанная на биопринтере Allevi компанией 3D Systems
Биопечатные структуры, такие как органы на чипах, можно использовать для изучения функций человеческого тела вне тела в 3D. Геометрия трехмерной биопечатной структуры больше похожа на геометрию естественной биологической системы, чем на двухмерную модель in vitro . Структурное сходство может, в свою очередь, привести к более физиологически релевантным функциональным результатам. Никакая другая технология не обеспечивает такого уровня геометрической сложности инженерных тканей, как 3D-биопечать. Вот почему эта технология может полностью изменить то, как мы лечим болезни, заменив тестирование на животных и положив конец очереди на трансплантацию органов.
Геометрия трехмерной биопечатной структуры больше похожа на геометрию естественной биологической системы, чем на двухмерную модель in vitro . Структурное сходство может, в свою очередь, привести к более физиологически релевантным функциональным результатам. Никакая другая технология не обеспечивает такого уровня геометрической сложности инженерных тканей, как 3D-биопечать. Вот почему эта технология может полностью изменить то, как мы лечим болезни, заменив тестирование на животных и положив конец очереди на трансплантацию органов.
Как работает 3D-биопечать?
3D-биопечать начинается с модели структуры, которая воссоздается слой за слоем из биочернил либо смешивается с живыми клетками, либо засеивается клетками после завершения печати. Эти исходные модели могут быть взяты откуда угодно: компьютерная томография или магнитно-резонансная томография, компьютерная программа проектирования (САПР) или файл, загруженный из Интернета.
Этот файл 3D-модели затем загружается в слайсер — специализированную компьютерную программу, которая анализирует геометрию модели и создает ряд тонких слоев или срезов, которые формируют форму исходной модели при вертикальном расположении . Cura и slic3r являются примерами слайсеров, обычно используемых в 3D-печати. Allevi также имеет специализированный слайсер, оптимизированный специально для биопечати, встроенный в наше программное обеспечение Allevi Bioprint.
Cura и slic3r являются примерами слайсеров, обычно используемых в 3D-печати. Allevi также имеет специализированный слайсер, оптимизированный специально для биопечати, встроенный в наше программное обеспечение Allevi Bioprint.
После нарезки модели срезы преобразуются в данные пути , сохраняемые в виде файла G-кода, который можно отправить на 3D-биопринтер для печати. Биопринтер следует инструкциям в файле G-кода по порядку, включая инструкции по контролю температуры экструдеров, давления экструзии, температуры опорной плиты, интенсивности и частоты сшивания и, конечно же, траектории трехмерного движения, создаваемой слайсером. После того, как все команды G-кода выполнены, отпечаток готов, и его можно культивировать или засевать клетками в рамках биоисследования.
Почему важна биопечать?
Только в США более 120 000 человек находятся в очереди на получение органов, а другие испытывают хронические проблемы из-за долгосрочных повреждающих последствий посттрансплантационной иммуносупрессии. Существует большая и растущая потребность в альтернативе очереди на трансплантацию органов. Научному сообществу уже удалось объединить междисциплинарные группы исследователей, врачей и инженеров для решения самых серьезных проблем со здоровьем человека, а 3D-биопечать — это новый захватывающий инструмент, который может устранить лист ожидания на трансплантацию органов.
Существует большая и растущая потребность в альтернативе очереди на трансплантацию органов. Научному сообществу уже удалось объединить междисциплинарные группы исследователей, врачей и инженеров для решения самых серьезных проблем со здоровьем человека, а 3D-биопечать — это новый захватывающий инструмент, который может устранить лист ожидания на трансплантацию органов.
Для фармацевтических разработок 3D-биопечать предлагает средства тестирования лекарств быстрее, с меньшими затратами и с большей биологической значимостью для людей, чем испытания на животных. В области биомедицинских устройств 3D-биопечать позволила разработать новые разработки, такие как сахарные стенты, помогающие хирургам соединять вены с меньшим количеством осложнений, а также системы для улучшенной доставки лекарств.
По мере развития биопечати станет возможным использовать собственные клетки пациента для 3D-печати кожных и костных трансплантатов, заплат для органов и даже полных замещающих органов.


 с.)
с.) GK 827 A8 Sturm 7. лс за 38550 р в Анапе
GK 827 A8 Sturm 7. лс за 38550 р в Анапе


 Однако многие специалисты предпочитают работать именно с металлом из-за прочности изделий и минимальной внешней обработки.
Однако многие специалисты предпочитают работать именно с металлом из-за прочности изделий и минимальной внешней обработки. Эти материалы подходят для изготовления предметов искусства, маленьких фигурок, архитектурных элементов.
Эти материалы подходят для изготовления предметов искусства, маленьких фигурок, архитектурных элементов.
 Часто из металла фрезеруют не мастер модель, а уже готовую матрицу, она имеет высокую надежность, стабильные параметры в широком диапазоне температур.
Часто из металла фрезеруют не мастер модель, а уже готовую матрицу, она имеет высокую надежность, стабильные параметры в широком диапазоне температур.




 В этом расчете учтите не менее 1/2″ пространства.
В этом расчете учтите не менее 1/2″ пространства.


 У этого нет специальной цели, вместо этого используйте что угодно другое — не рискуйте повредить свой идеальный лист для печати 🙂
У этого нет специальной цели, вместо этого используйте что угодно другое — не рискуйте повредить свой идеальный лист для печати 🙂 Этот формовочный материал подходит как для небольших, детализированных слепков, так и для крупных объектов (например, статуй). Вакуумный насос не требуется из-за отличной текучести и низкой вязкости. Силиконовый каучук можно как наливать, так и наносить кистью (с добавлением в смесь загустителя), хотя есть и лучшие варианты нанесения кистью, например, Smooth-on, упомянутый выше.
Этот формовочный материал подходит как для небольших, детализированных слепков, так и для крупных объектов (например, статуй). Вакуумный насос не требуется из-за отличной текучести и низкой вязкости. Силиконовый каучук можно как наливать, так и наносить кистью (с добавлением в смесь загустителя), хотя есть и лучшие варианты нанесения кистью, например, Smooth-on, упомянутый выше. Другими словами, если вы посмотрите на пресс-форму прямо сверху, вы должны увидеть всю внутреннюю поверхность , ничего не спрятанного «за углом». Эти выступы могут позже привести к застреванию мастер-модели или окончательной отливки в форме. К счастью, одним из больших преимуществ силиконовой резины является ее эластичность — она немного деформируется, когда мы сгибаем и скручиваем ее, чтобы вынуть готовый слепок. Это означает, что мы могли позволить себе определенный уровень выступов. Правильно отлитая модель должна выскочить почти самопроизвольно после легкого нажатия на форму.
Другими словами, если вы посмотрите на пресс-форму прямо сверху, вы должны увидеть всю внутреннюю поверхность , ничего не спрятанного «за углом». Эти выступы могут позже привести к застреванию мастер-модели или окончательной отливки в форме. К счастью, одним из больших преимуществ силиконовой резины является ее эластичность — она немного деформируется, когда мы сгибаем и скручиваем ее, чтобы вынуть готовый слепок. Это означает, что мы могли позволить себе определенный уровень выступов. Правильно отлитая модель должна выскочить почти самопроизвольно после легкого нажатия на форму. Напечатать слои не проблема (с точки зрения извлечения из формы), но они, конечно, будут видны на готовой отливке. значит печать из смолы больше подходит — я использовал принтер Original Prusa SL1.
Напечатать слои не проблема (с точки зрения извлечения из формы), но они, конечно, будут видны на готовой отливке. значит печать из смолы больше подходит — я использовал принтер Original Prusa SL1. Заливочный канал и вентиляционные отверстия в форме мы прорежем позже, перед самой отливкой.
Заливочный канал и вентиляционные отверстия в форме мы прорежем позже, перед самой отливкой. 4 стенки по периметру сделали корпус достаточно прочным.
4 стенки по периметру сделали корпус достаточно прочным.


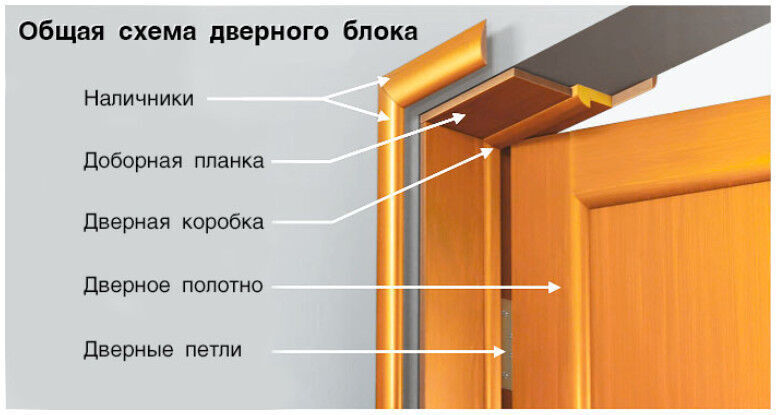





 В деревянном доме именно наличники из древесины будут смотреться наиболее органично. Деревянные наличники можно украсить традиционной резьбой – ведь много столетий наши предки обрамляли окна резными деревянными украшениями на окнах и ставнях. Резьба включала многочисленные символы, считалось, что эти знаки охраняют дом от злых духов и приносят его жильцам удачу и здоровье. Для наличников используют разные породы дерева;
В деревянном доме именно наличники из древесины будут смотреться наиболее органично. Деревянные наличники можно украсить традиционной резьбой – ведь много столетий наши предки обрамляли окна резными деревянными украшениями на окнах и ставнях. Резьба включала многочисленные символы, считалось, что эти знаки охраняют дом от злых духов и приносят его жильцам удачу и здоровье. Для наличников используют разные породы дерева;
 Часто наличникам оставляли естественный цвет дерева, но во многих районах окрашивали, иногда в несколько цветов – синий с белым, голубой, зеленый, коричневый, желтый… Целый пласт культуры наших прадедов связан с отделкой оконных наличников.
Часто наличникам оставляли естественный цвет дерева, но во многих районах окрашивали, иногда в несколько цветов – синий с белым, голубой, зеленый, коричневый, желтый… Целый пласт культуры наших прадедов связан с отделкой оконных наличников. Рекомендуют вначале вымерять и обрезать боковые наличники. Верхнюю планку желательно обрезать с запасом, чтобы не допустить образования щелей, и при необходимости подогнать размеры в процессе работы.
Рекомендуют вначале вымерять и обрезать боковые наличники. Верхнюю планку желательно обрезать с запасом, чтобы не допустить образования щелей, и при необходимости подогнать размеры в процессе работы. Из деревянных заготовок можно вырезать удивительные узоры, которые напомнят о старинных теремах, о верованиях и оберегах наших предков.
Из деревянных заготовок можно вырезать удивительные узоры, которые напомнят о старинных теремах, о верованиях и оберегах наших предков.

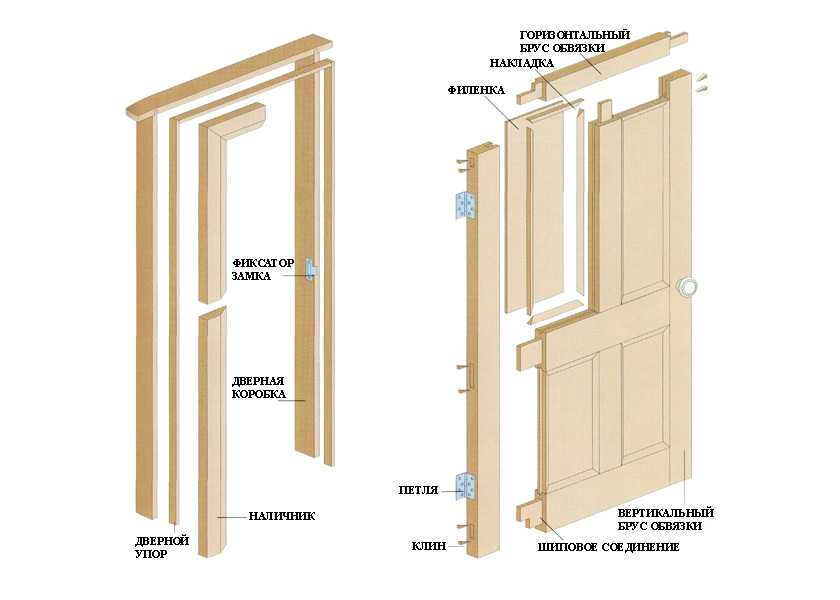



 Такие наличники делают его визуально монолитным, оставляя крепления незаметными. Они предназначены для обустройства нестандартных проемов.
Такие наличники делают его визуально монолитным, оставляя крепления незаметными. Они предназначены для обустройства нестандартных проемов.
 Окончательная установка подготовленных наличников на дверь возможна только после их тщательной подгонки по размерам с соблюдением прямых углов и минимальными зазорами соединяемых частей.
Окончательная установка подготовленных наличников на дверь возможна только после их тщательной подгонки по размерам с соблюдением прямых углов и минимальными зазорами соединяемых частей. Такую же дополнительную подготовку необходимо произвести при использовании в качестве крепежа саморезов. Но для них потребуются отверстия несколько большего диаметра, чтобы утопить шляпки, которые впоследствии закрывают заглушками в тон отделке, либо заделывают акриловой шпаклевкой перед покраской.
Такую же дополнительную подготовку необходимо произвести при использовании в качестве крепежа саморезов. Но для них потребуются отверстия несколько большего диаметра, чтобы утопить шляпки, которые впоследствии закрывают заглушками в тон отделке, либо заделывают акриловой шпаклевкой перед покраской.
 Они становятся обрамлением проема, визуально дверь становится единым целым. Однако нужны они и по другой причине – это приспособление отлично закрывает все щели, оставшиеся после монтажа, исправляет несовершенства монтажа и мелкие дефекты конструкции.
Они становятся обрамлением проема, визуально дверь становится единым целым. Однако нужны они и по другой причине – это приспособление отлично закрывает все щели, оставшиеся после монтажа, исправляет несовершенства монтажа и мелкие дефекты конструкции.
 У этого варианта есть свои плюсы и минусы: они выглядят намного оригинальнее и красивее, но если их установить без обрезки, то средняя часть будет сильно выступать относительно нижнего торца. В этом случае красота требует жертв – придется заниматься оформлением угла в 45 градусов и тут нужна аккуратность с аккуратностью.
У этого варианта есть свои плюсы и минусы: они выглядят намного оригинальнее и красивее, но если их установить без обрезки, то средняя часть будет сильно выступать относительно нижнего торца. В этом случае красота требует жертв – придется заниматься оформлением угла в 45 градусов и тут нужна аккуратность с аккуратностью.
 Возможно, что в процессе инструмент начнет двигаться и линия реза выйдет волнистой или криволинейной, в этом случае используйте ножовку и исправьте ситуацию.
Возможно, что в процессе инструмент начнет двигаться и линия реза выйдет волнистой или криволинейной, в этом случае используйте ножовку и исправьте ситуацию.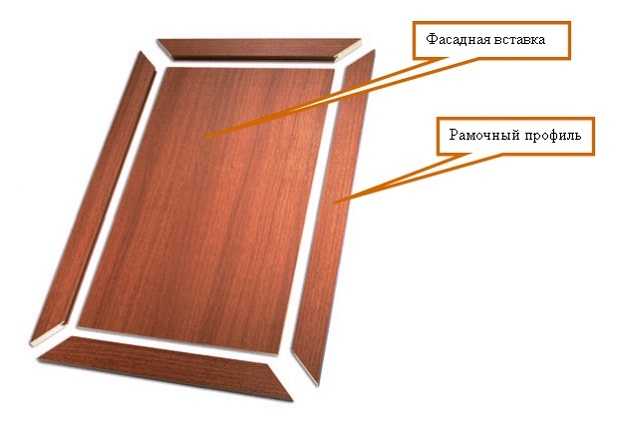 Конечно, интересующий многих вариант – это клей. Удобство и долговечность – это плюсы, но когда вы решите демонтировать, вам придется полностью повредить установленную накладку.
Конечно, интересующий многих вариант – это клей. Удобство и долговечность – это плюсы, но когда вы решите демонтировать, вам придется полностью повредить установленную накладку. Сначала не прибиваем «туго», а лишь слегка придавливаем двумя гвоздями: одним снизу, другим посередине.
Сначала не прибиваем «туго», а лишь слегка придавливаем двумя гвоздями: одним снизу, другим посередине. Наличники здесь устанавливаются по тому же принципу, только делать отступы не нужно, ведь никакие петли нам не мешают.
Наличники здесь устанавливаются по тому же принципу, только делать отступы не нужно, ведь никакие петли нам не мешают. Эта статья как раз для этого и предназначена – помочь установить наличники на двери своими руками.
Эта статья как раз для этого и предназначена – помочь установить наличники на двери своими руками.
 Главное помнить при нарезании этого паза — осторожность и еще раз осторожность, так как иначе можно просто расколоть корпус . Глубина этого так называемого срединного выделения зависит от толщины наличника. Образец рекомендуется углубить стамеской.
Главное помнить при нарезании этого паза — осторожность и еще раз осторожность, так как иначе можно просто расколоть корпус . Глубина этого так называемого срединного выделения зависит от толщины наличника. Образец рекомендуется углубить стамеской. Имейте в виду, что специалисты рекомендуют вбивать декоративные гвозди примерно через каждые 50 сантиметров. Эти гвозди можно вбивать почти в самый край наличников, что сохранит известную эстетику.
Имейте в виду, что специалисты рекомендуют вбивать декоративные гвозди примерно через каждые 50 сантиметров. Эти гвозди можно вбивать почти в самый край наличников, что сохранит известную эстетику.
 Так постройка будет смотреться гармонично и красиво. При строительстве из современных материалов уместна пластиковая и металлическая отделка.
Так постройка будет смотреться гармонично и красиво. При строительстве из современных материалов уместна пластиковая и металлическая отделка.


 Но у них есть и практическая задача – закрыть щель между оконным или дверным проемом и коробкой, поэтому необходимо установить отделка при внешней отделке в любом случае, вне зависимости от выбранного материала и дизайна.
Но у них есть и практическая задача – закрыть щель между оконным или дверным проемом и коробкой, поэтому необходимо установить отделка при внешней отделке в любом случае, вне зависимости от выбранного материала и дизайна.


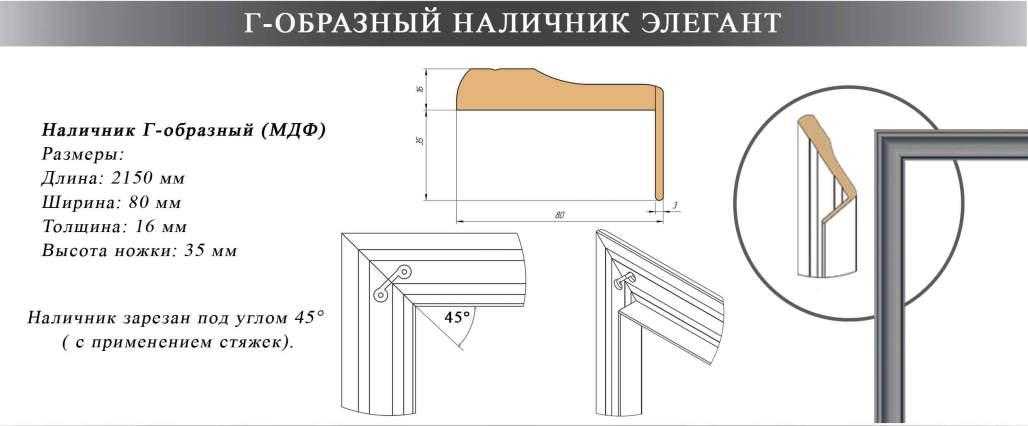 Фигурный профиль может быть угловатым, криволинейным, с несколькими выступами, пазами, закруглениями. Изготавливают такие предметы декора из пластика, алюминия или дерева.
Фигурный профиль может быть угловатым, криволинейным, с несколькими выступами, пазами, закруглениями. Изготавливают такие предметы декора из пластика, алюминия или дерева.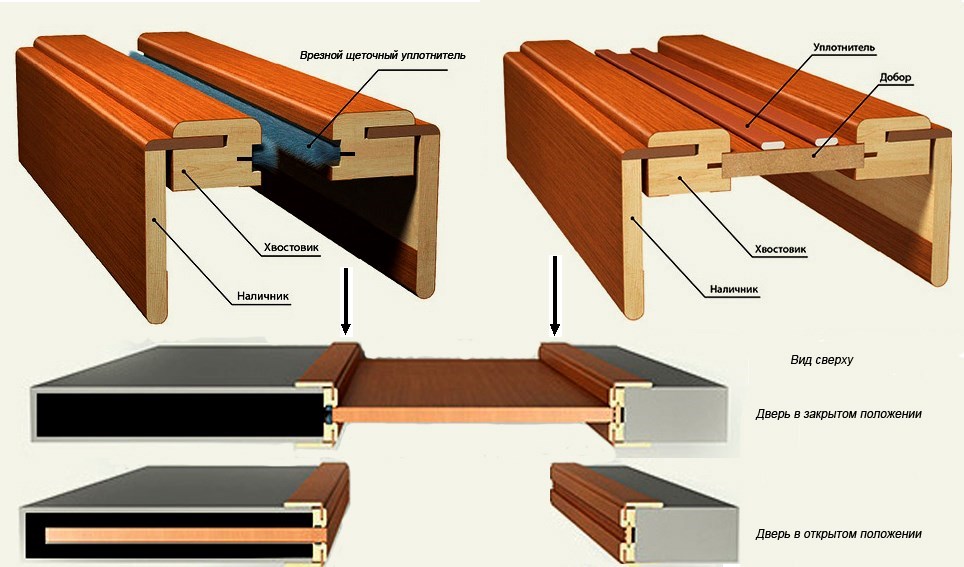
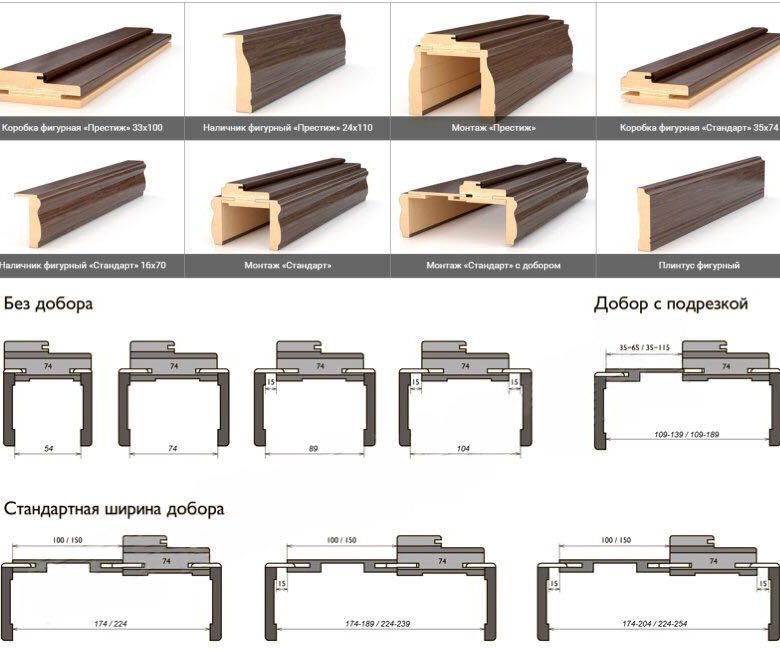 Материал изготавливается путем прессования измельченных древесных волокон, которые затем покрываются сверху цветной защитной пленкой. Разнообразие цветов и фактур поверхности позволяет выполнить любой дизайн, плиты МДФ легко режутся и крепятся к деревянной поверхности. За ними очень легко ухаживать – достаточно протирать их влажной тряпкой.
Материал изготавливается путем прессования измельченных древесных волокон, которые затем покрываются сверху цветной защитной пленкой. Разнообразие цветов и фактур поверхности позволяет выполнить любой дизайн, плиты МДФ легко режутся и крепятся к деревянной поверхности. За ними очень легко ухаживать – достаточно протирать их влажной тряпкой. Он прослужит долго, не боится влаги, перепадов температур и механических повреждений. Кроме того, есть выбор разных цветов.
Он прослужит долго, не боится влаги, перепадов температур и механических повреждений. Кроме того, есть выбор разных цветов.
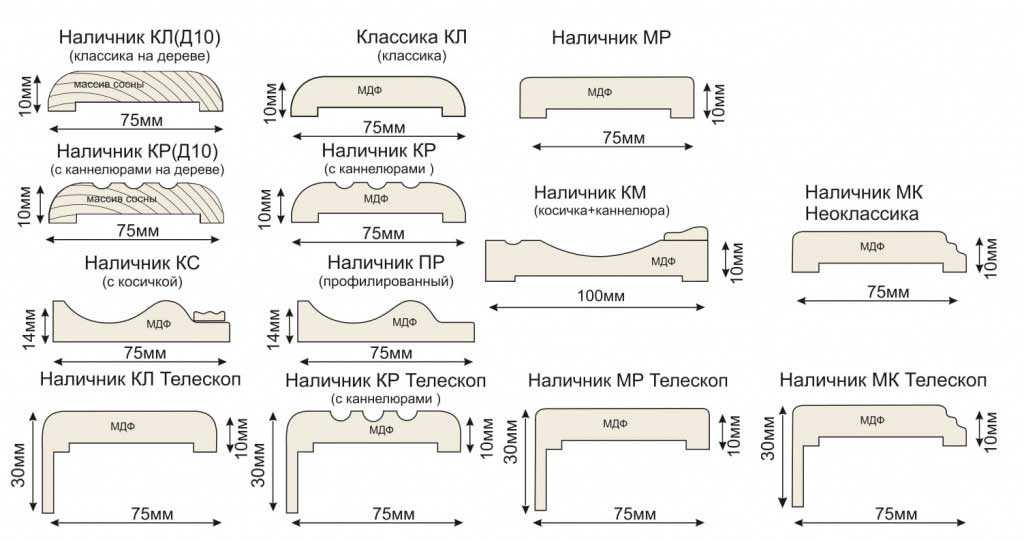 Эти размеры позволяют надежно закрыть щели в оконных и дверных проемах. Для строений с деревянными стенами, которые в зависимости от времени года и погодных условий меняют свою толщину, стоит покупать телескопические наличники со сменными размерами.
Эти размеры позволяют надежно закрыть щели в оконных и дверных проемах. Для строений с деревянными стенами, которые в зависимости от времени года и погодных условий меняют свою толщину, стоит покупать телескопические наличники со сменными размерами.
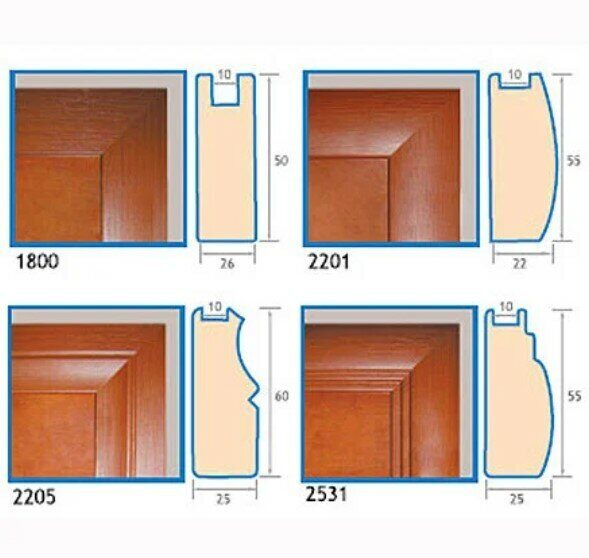
 Стандартная длина отделочных гвоздей 4 см, необходимо подобрать такую, чтобы они были на 1,5 см длиннее обрезных. Крепеж вбивается на расстоянии 0,5 м друг от друга, чтобы шляпка не утонула в бруске, можно использовать добойник. Преимущество отделочных гвоздей еще и в том, что впоследствии накладку легко демонтировать.
Стандартная длина отделочных гвоздей 4 см, необходимо подобрать такую, чтобы они были на 1,5 см длиннее обрезных. Крепеж вбивается на расстоянии 0,5 м друг от друга, чтобы шляпка не утонула в бруске, можно использовать добойник. Преимущество отделочных гвоздей еще и в том, что впоследствии накладку легко демонтировать. Сначала в кожухе сверлятся отверстия нужной ширины, затем делаются углубления под колпак. После этого элемент крепится на саморезы к стене дома.
Сначала в кожухе сверлятся отверстия нужной ширины, затем делаются углубления под колпак. После этого элемент крепится на саморезы к стене дома.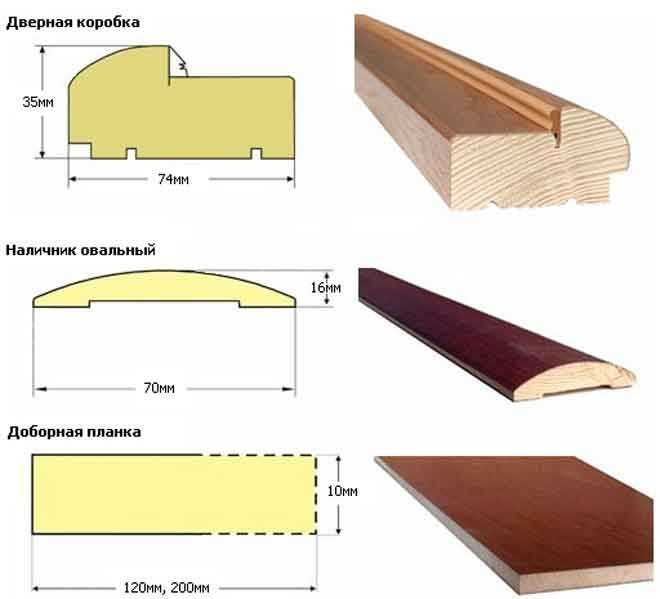 Обязательно проверьте вертикальный уровень стен: они вместе с коробом должны лежать строго в одной плоскости. Невыполнение этого требования не приведет к эффективному закрытию зазоров, они могут выглядеть неровными на расстоянии и со временем деформироваться.
Обязательно проверьте вертикальный уровень стен: они вместе с коробом должны лежать строго в одной плоскости. Невыполнение этого требования не приведет к эффективному закрытию зазоров, они могут выглядеть неровными на расстоянии и со временем деформироваться.
 Основная проблема здесь – стыковка углов. Сопряжение вертикальных и горизонтальных планок может быть под прямым углом, но выглядит это не очень красиво. Каждую из деталей лучше всего выпилить под углом 45 градусов торцовочной пилой с помощью столярного бруса и затем соединить их точно по проему.
Основная проблема здесь – стыковка углов. Сопряжение вертикальных и горизонтальных планок может быть под прямым углом, но выглядит это не очень красиво. Каждую из деталей лучше всего выпилить под углом 45 градусов торцовочной пилой с помощью столярного бруса и затем соединить их точно по проему. На производство массива натуральной извести на всю продукцию распространяется гарантия. Изделия имеют разнообразную расцветку под любой фасад деревянного дома, идеально отшлифованы и обработаны лаком, стойким к природным воздействиям. Такие декоративные детали могут долго прослужить в загородном доме.
На производство массива натуральной извести на всю продукцию распространяется гарантия. Изделия имеют разнообразную расцветку под любой фасад деревянного дома, идеально отшлифованы и обработаны лаком, стойким к природным воздействиям. Такие декоративные детали могут долго прослужить в загородном доме.
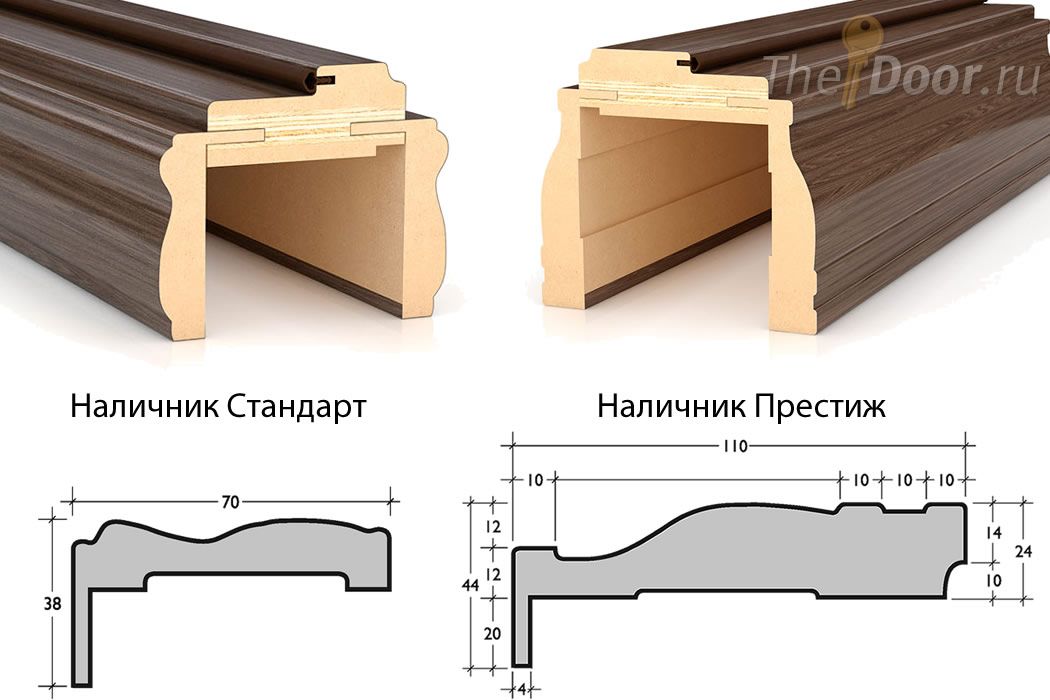 Резные наличники и другие аксессуары представляют собой изделия ручной работы. Продукция этих компаний по большей части получает многочисленные положительные отзывы покупателей.
Резные наличники и другие аксессуары представляют собой изделия ручной работы. Продукция этих компаний по большей части получает многочисленные положительные отзывы покупателей. Для крепежа лучше всего выбирать жидкие или финишные гвозди. Время от времени отделку следует не только очищать, но и наносить на поверхность дополнительный слой лака или краски, чтобы избавиться от трещин.
Для крепежа лучше всего выбирать жидкие или финишные гвозди. Время от времени отделку следует не только очищать, но и наносить на поверхность дополнительный слой лака или краски, чтобы избавиться от трещин.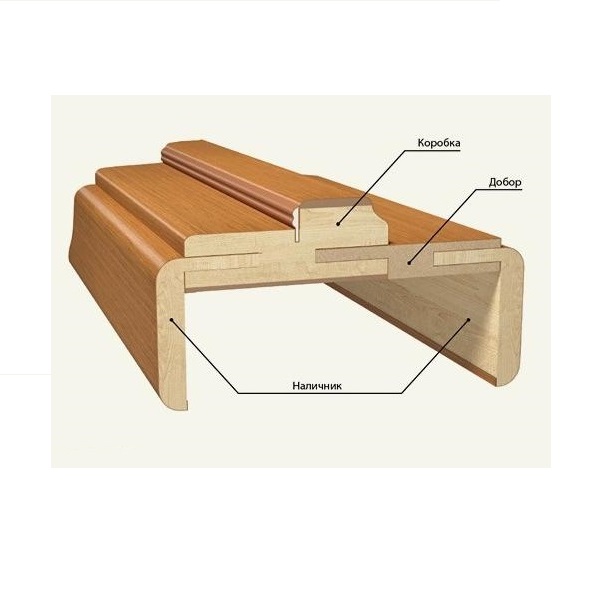
 0
0 5
5 4
4 36 МБ)
36 МБ) 0 Ач в комплекте для безостановочной работы
0 Ач в комплекте для безостановочной работы 0 А*ч
0 А*ч 00 единиц
00 единиц 2 ASI
2 ASI 00 единиц
00 единиц


 00 единиц
00 единиц 00 единиц
00 единиц



 разм. резки □ под 90º – 180х300 мм
разм. резки □ под 90º – 180х300 мм
 Трубка подачи СОЖ
Трубка подачи СОЖ 75
75 toFixed(2)}% скидка
toFixed(2)}% скидка описание}
описание} value }
value } 8amp Ballast 120v-ac 210w Lighting D237617
8amp Ballast 120v-ac 210w Lighting D237617 toFixed(2)}% скидка
toFixed(2)}% скидка




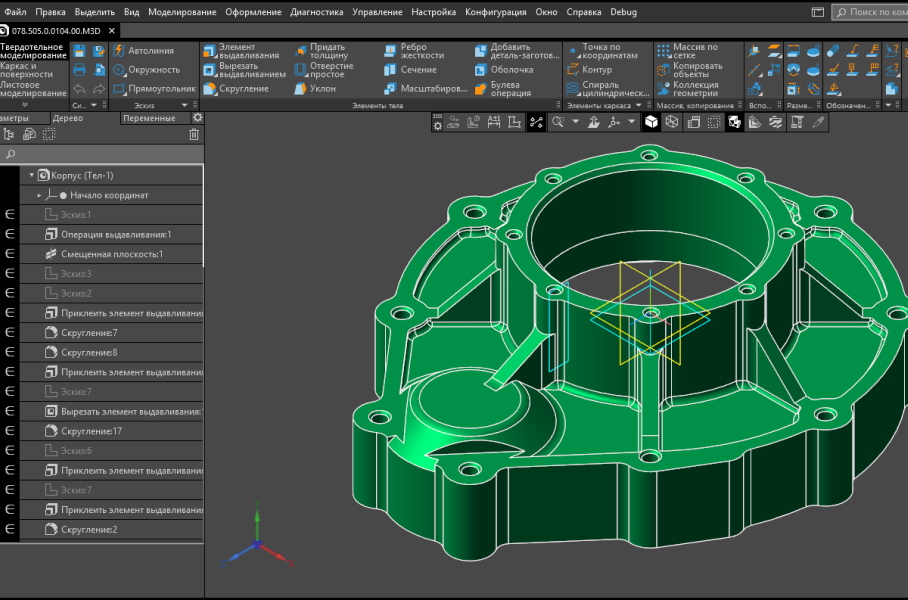
 0.3 необходимо установить Java 6 или более позднюю версию. В процессе установки 3D редактора мастер установки предложит скачать необходимую программу и посоветует сайт.
0.3 необходимо установить Java 6 или более позднюю версию. В процессе установки 3D редактора мастер установки предложит скачать необходимую программу и посоветует сайт. 7 ограничены, но их хватает для создания простого интерьера, используя готовую библиотеку объектов.
7 ограничены, но их хватает для создания простого интерьера, используя готовую библиотеку объектов. Программа проста в обращении и понятна простому пользователю, никогда не работавшему в редакторах трехмерного пространства.
Программа проста в обращении и понятна простому пользователю, никогда не работавшему в редакторах трехмерного пространства.
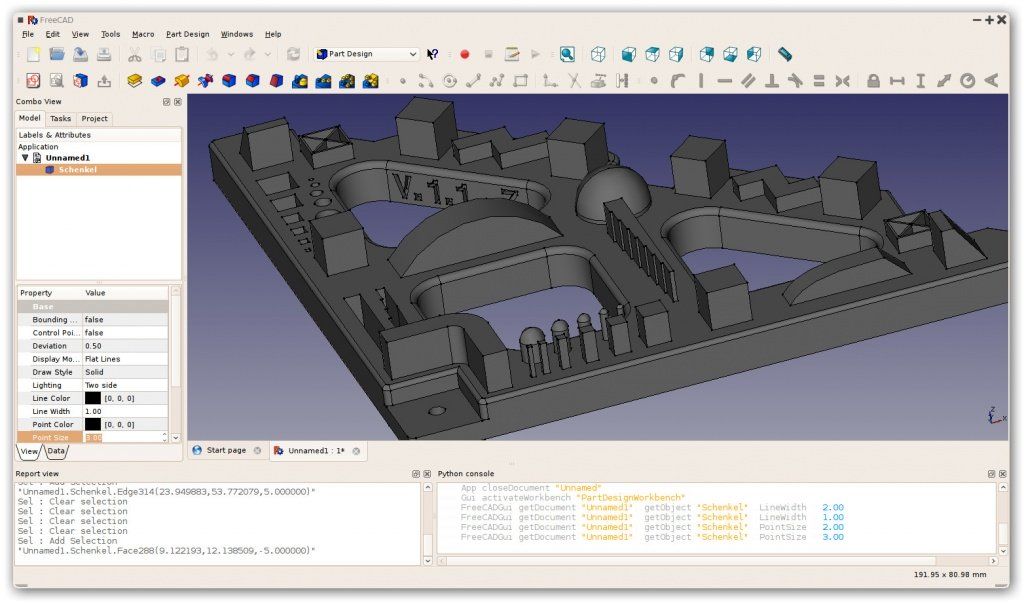
 Для создания анимации применяется мойный движок, позволяющий создавать сложные сцены.
Для создания анимации применяется мойный движок, позволяющий создавать сложные сцены.
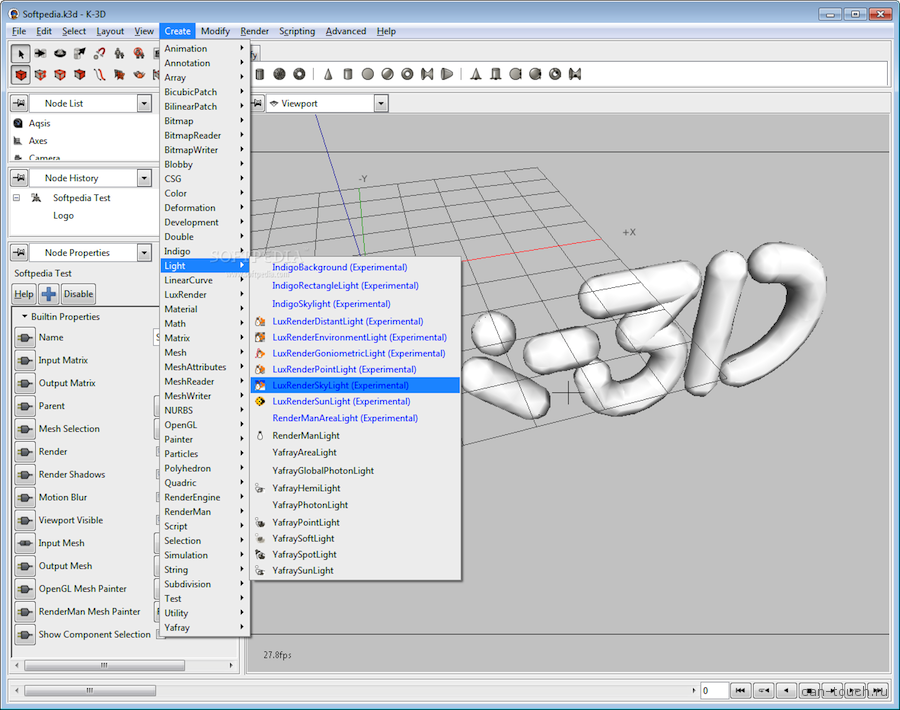 Благодаря этому после освоения программы человек получает полную свободу действий в создании объектов и сцен.
Благодаря этому после освоения программы человек получает полную свободу действий в создании объектов и сцен.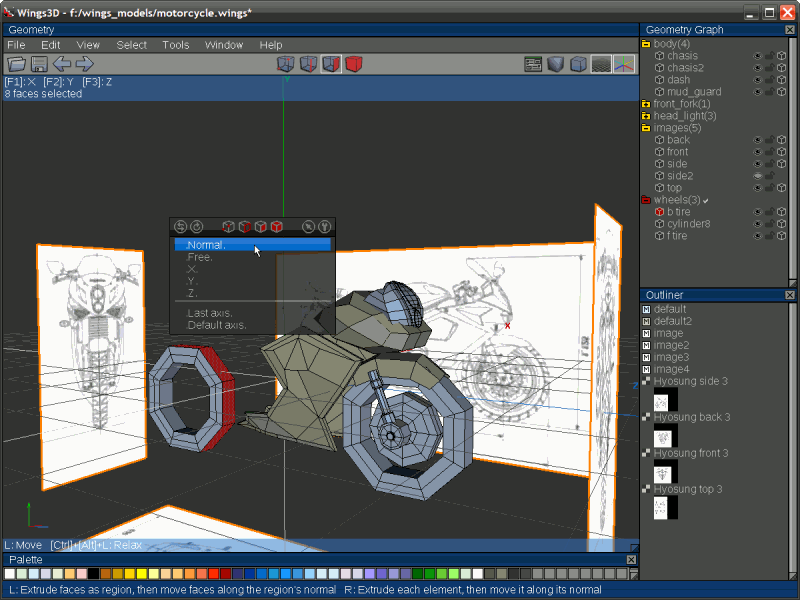
 Представленные в обзоре приложения полностью бесплатны или имеют бесплатные версии для студентов, преподавателей и проектов с открытым исходным кодом.
Представленные в обзоре приложения полностью бесплатны или имеют бесплатные версии для студентов, преподавателей и проектов с открытым исходным кодом.
 Он позволяет получать информацию для печати, а также изменять параметры работы устройства в режиме реального времени через ПК. Часто Слайсер и хост объединены в одно ПО для 3D печати, которое поставляется производителем принтера.
Он позволяет получать информацию для печати, а также изменять параметры работы устройства в режиме реального времени через ПК. Часто Слайсер и хост объединены в одно ПО для 3D печати, которое поставляется производителем принтера.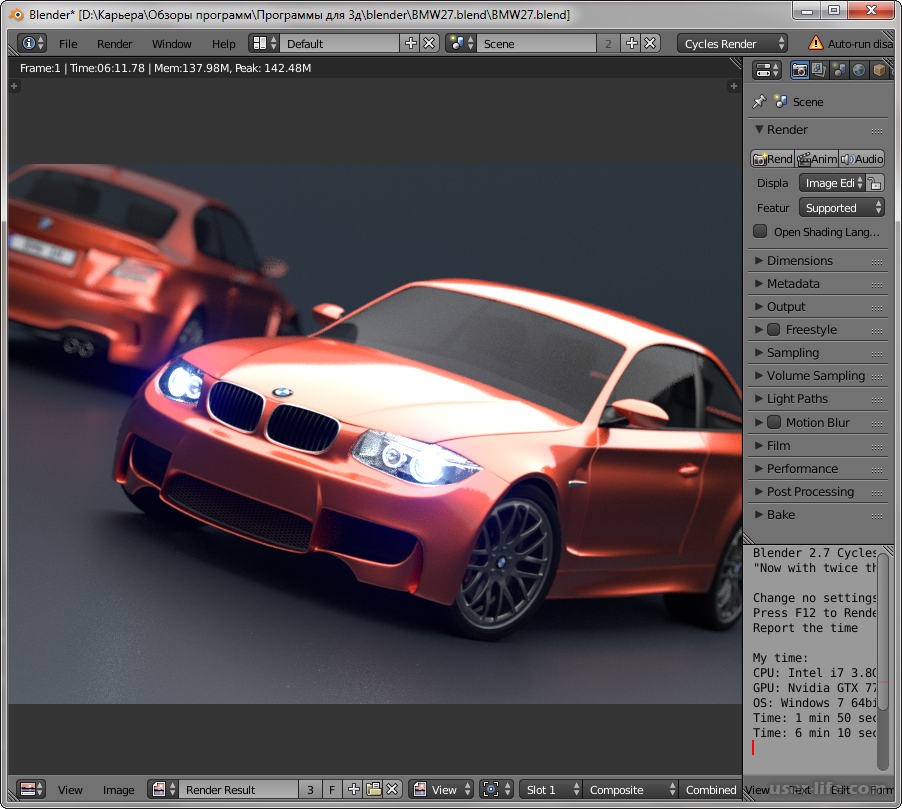 Однако ее функционал подходит для использования совместно с другими 3D принтерами. Поскольку это ПО является одним из самых популярный среди мейкеров, можно не тратить время на настройки профиля — для большинства принтеров их можно найти в самой программе.
Однако ее функционал подходит для использования совместно с другими 3D принтерами. Поскольку это ПО является одним из самых популярный среди мейкеров, можно не тратить время на настройки профиля — для большинства принтеров их можно найти в самой программе.

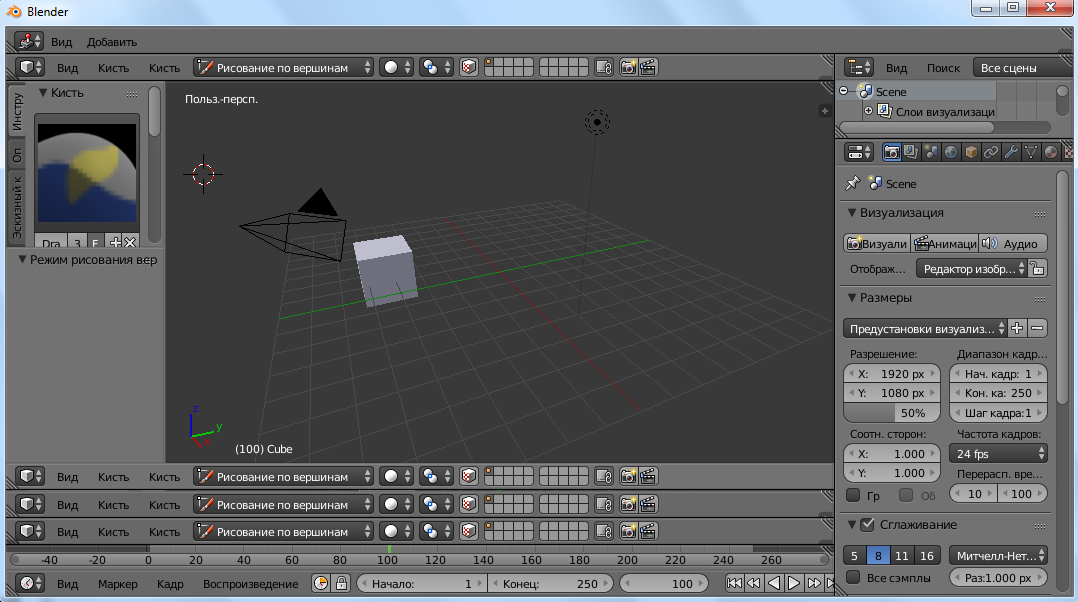
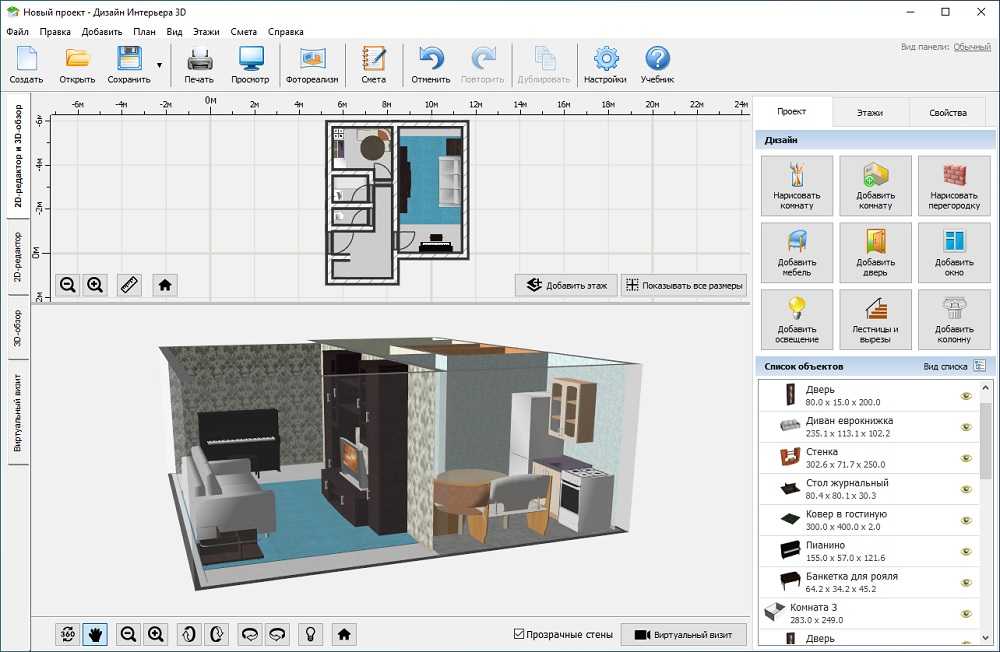 Полученные 3D модели легко экспортировать в слайсер и распечатать. Таким образом, программа позволяет контролировать весь процесс — от создания модели, до ее нарезки и отправки в печать.
Полученные 3D модели легко экспортировать в слайсер и распечатать. Таким образом, программа позволяет контролировать весь процесс — от создания модели, до ее нарезки и отправки в печать.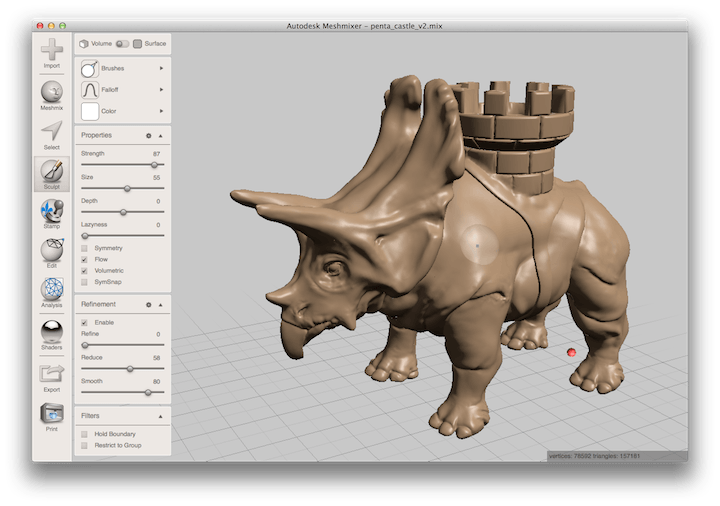 Именно поэтому 3DPrinterOS подходит для небольшого бизнеса, обучения, производства и дизайна.
Именно поэтому 3DPrinterOS подходит для небольшого бизнеса, обучения, производства и дизайна. сайт KISSlicer
сайт KISSlicer С помощью программы можно быстро загрузить STL файлы, нарезать их, а затем подготовить G-код к печати. В браузерной программе можно воспользоваться практически всеми опциями, которые предлагает IceSL.
С помощью программы можно быстро загрузить STL файлы, нарезать их, а затем подготовить G-код к печати. В браузерной программе можно воспользоваться практически всеми опциями, которые предлагает IceSL.
 Все это позволяет сделать плавные переходы от плотного к легкому заполнению и градацию толщины слоев от мелкого к крупному.
Все это позволяет сделать плавные переходы от плотного к легкому заполнению и градацию толщины слоев от мелкого к крупному. На странице сообщества можно найти множество надстроек, которые будут полезны при печати.
На странице сообщества можно найти множество надстроек, которые будут полезны при печати.

 Возможности софта помогают проверять, визуализировать, восстанавливать и преобразовывать сетки, и даже объединять модели в твердые тела и заделывать дыры.
Возможности софта помогают проверять, визуализировать, восстанавливать и преобразовывать сетки, и даже объединять модели в твердые тела и заделывать дыры.
 Программа подойдет для тех, кто хочет улучшить свои навыки в проектировании, при этом не сильно углубляясь в детали.
Программа подойдет для тех, кто хочет улучшить свои навыки в проектировании, при этом не сильно углубляясь в детали.
 Программа подойдет для дизайна изделий, машиностроения, архитектуры и других областей.
Программа подойдет для дизайна изделий, машиностроения, архитектуры и других областей. Этот софт — не лучший выбор для новичка, но идеальна для тех, кто знаком с концепциями 3D моделирования и хочет создавать более сложные модели.
Этот софт — не лучший выбор для новичка, но идеальна для тех, кто знаком с концепциями 3D моделирования и хочет создавать более сложные модели.

 Больше не бойтесь, теперь вы можете начать 3D-моделирование на своих мобильных устройствах ! Да, вы можете начать использовать приложение для 3D-моделирования для устройств iOS, Android или Windows . Есть много вариантов в зависимости от ваших навыков. Какое из наших 15 лучших приложений для 3D-моделирования лучше всего подходит для вашего следующего проекта? Давай выясним!
Больше не бойтесь, теперь вы можете начать 3D-моделирование на своих мобильных устройствах ! Да, вы можете начать использовать приложение для 3D-моделирования для устройств iOS, Android или Windows . Есть много вариантов в зависимости от ваших навыков. Какое из наших 15 лучших приложений для 3D-моделирования лучше всего подходит для вашего следующего проекта? Давай выясним!
 В зависимости от того, начинаете ли вы свое 3D-приключение, хотите просто повеселиться или являетесь профессионалом, ищущим больше мобильных решений, наш список 15 лучших приложений для моделирования для мобильных устройств должен дать вам ответ. Или, может быть, вы хотите напечатать свои модели на 3D-принтере?
В зависимости от того, начинаете ли вы свое 3D-приключение, хотите просто повеселиться или являетесь профессионалом, ищущим больше мобильных решений, наш список 15 лучших приложений для моделирования для мобильных устройств должен дать вам ответ. Или, может быть, вы хотите напечатать свои модели на 3D-принтере?
 Благодаря доступности Shapr3D Sync на базе Shapr3D Cloud, позволяющей легко импортировать/экспортировать и использовать на нескольких платформах, Shapr3D идеально вписывается в ваш существующий рабочий процесс.
Благодаря доступности Shapr3D Sync на базе Shapr3D Cloud, позволяющей легко импортировать/экспортировать и использовать на нескольких платформах, Shapr3D идеально вписывается в ваш существующий рабочий процесс. shapr3d.com/terms-of-use
shapr3d.com/terms-of-use 
 Это привлекло мое внимание, потому что это было программное обеспечение, в которое я влюбился, когда учился в школе механического проектирования. Так что одно это заставило меня скачать и попробовать приложение. Я попробовал бесплатную версию, которая полностью функциональна, когда дело доходит до дизайна, но ограничивает определенные функции и количество дизайнов, которые можно создать. После нескольких вариантов дизайна, который я завершил. Я решил стиснуть зубы и подписаться на ежемесячную полную версию. До сих пор я рад, что вы получили дополнительные функции, чтобы не только сохранить дизайн без ограничения количества, но и настроить цвета, чтобы дизайн выглядел и чувствовал себя более реальным, чтобы лучше понять видение продукта, который вы планируете создать. Это интуитивно понятное приложение, но у меня есть обширный опыт работы с Solid-works и AutoCad, и это очень помогло при проектировании, потому что эта программа представляет собой небольшую смесь как приложений, так и инструментов, похожих на смесь каждой из этих двух программ.
Это привлекло мое внимание, потому что это было программное обеспечение, в которое я влюбился, когда учился в школе механического проектирования. Так что одно это заставило меня скачать и попробовать приложение. Я попробовал бесплатную версию, которая полностью функциональна, когда дело доходит до дизайна, но ограничивает определенные функции и количество дизайнов, которые можно создать. После нескольких вариантов дизайна, который я завершил. Я решил стиснуть зубы и подписаться на ежемесячную полную версию. До сих пор я рад, что вы получили дополнительные функции, чтобы не только сохранить дизайн без ограничения количества, но и настроить цвета, чтобы дизайн выглядел и чувствовал себя более реальным, чтобы лучше понять видение продукта, который вы планируете создать. Это интуитивно понятное приложение, но у меня есть обширный опыт работы с Solid-works и AutoCad, и это очень помогло при проектировании, потому что эта программа представляет собой небольшую смесь как приложений, так и инструментов, похожих на смесь каждой из этих двух программ. Apple Pencil необходим для этого, потому что он действует как мышь/курсер и очень точен.
Apple Pencil необходим для этого, потому что он действует как мышь/курсер и очень точен. Что было бы хорошо, честно говоря, со всеми созданными учебниками, которые так здорово показывают вам, как использовать приложение, я думаю, оно того заслуживает, но не за 300 долларов, которые они просят. Я бы с радостью заплатил 10 долларов или около того в месяц за средний уровень, и меня удивляет, что они этого не делают, поскольку в анкете, которую вы заполняете в начале, спрашивается, используете ли вы его для хобби или никогда раньше не занимались 3D-моделированием. . Если он предназначен только для профессионалов, и вы не хотите, чтобы его использовали любители, то зачем даже спрашивать, являются ли они одними из них? Я даже не прошу вас сделать все функции бесплатными, как это делает fusion 360, просто снизить стоимость для непрофессионалов, если вы действительно хотите, чтобы любители и непрофессионалы также использовали его
Что было бы хорошо, честно говоря, со всеми созданными учебниками, которые так здорово показывают вам, как использовать приложение, я думаю, оно того заслуживает, но не за 300 долларов, которые они просят. Я бы с радостью заплатил 10 долларов или около того в месяц за средний уровень, и меня удивляет, что они этого не делают, поскольку в анкете, которую вы заполняете в начале, спрашивается, используете ли вы его для хобби или никогда раньше не занимались 3D-моделированием. . Если он предназначен только для профессионалов, и вы не хотите, чтобы его использовали любители, то зачем даже спрашивать, являются ли они одними из них? Я даже не прошу вас сделать все функции бесплатными, как это делает fusion 360, просто снизить стоимость для непрофессионалов, если вы действительно хотите, чтобы любители и непрофессионалы также использовали его Для получения дополнительной информации см. политику конфиденциальности разработчика.
Для получения дополнительной информации см. политику конфиденциальности разработчика.
 373.501 сливного насоса ДАО-13 стиральной машины Вятка
373.501 сливного насоса ДАО-13 стиральной машины Вятка под авар. слив)
под авар. слив)
 ..
.. Вал протыкает внутреннее «кольцо» или внутреннюю часть корпуса насоса.
Вал протыкает внутреннее «кольцо» или внутреннюю часть корпуса насоса.

 W. Chesterton Company за предоставленный ниже 8,5-минутный видеоролик, в котором показана замена сальника на сальниковую коробку .
W. Chesterton Company за предоставленный ниже 8,5-минутный видеоролик, в котором показана замена сальника на сальниковую коробку .

 ..
..
 назад» в «насосную сторону» помпы!
назад» в «насосную сторону» помпы!






 Надежность сальника имеет решающее значение для состояния и производительности всей программы гидроизоляции. Чем выше производительность и надежность программы гидроизоляции, тем лучше состояние внутренних компонентов насоса, включая сальник.
Надежность сальника имеет решающее значение для состояния и производительности всей программы гидроизоляции. Чем выше производительность и надежность программы гидроизоляции, тем лучше состояние внутренних компонентов насоса, включая сальник. Это создает уплотнение.
Это создает уплотнение. Надлежащая упаковка должна в первую очередь устранять утечки, что приводит к сокращению времени простоя оборудования из-за проблем с сальниковой водой.
Надлежащая упаковка должна в первую очередь устранять утечки, что приводит к сокращению времени простоя оборудования из-за проблем с сальниковой водой. Прогиб вызывает преждевременный износ набивки и механического уплотнения. Кроме того, труднее контролировать использование промывочной воды и утечку при отклонении.
Прогиб вызывает преждевременный износ набивки и механического уплотнения. Кроме того, труднее контролировать использование промывочной воды и утечку при отклонении. Эти компоненты включают горловину сальниковой коробки и/или втулки горловины, а также грундбуксу и фонарные кольца.
Эти компоненты включают горловину сальниковой коробки и/или втулки горловины, а также грундбуксу и фонарные кольца. Износ также может произойти, если персонал добавит уплотнительные кольца без полной перенабивки сальниковой камеры.
Износ также может произойти, если персонал добавит уплотнительные кольца без полной перенабивки сальниковой камеры. Для насосов учитывайте рабочую температуру, давление, скорость вращения вала и диапазон pH. Для клапанов учитывайте максимальную температуру линии, давление и диапазон pH.
Для насосов учитывайте рабочую температуру, давление, скорость вращения вала и диапазон pH. Для клапанов учитывайте максимальную температуру линии, давление и диапазон pH.

 график
график 00
00 график
график



 Разница давлений между синхронизацией выпускных и впускных клапанов и оборотами двигателя влияет на количество остаточного газа. Операция Клапан выпускной дроссельной заслонки увеличивает насосные потери и температуру выхлопных газов. Когда поток насоса регулируется гидравлическим дроссельным клапаном , кривая системы изменяется.
Разница давлений между синхронизацией выпускных и впускных клапанов и оборотами двигателя влияет на количество остаточного газа. Операция Клапан выпускной дроссельной заслонки увеличивает насосные потери и температуру выхлопных газов. Когда поток насоса регулируется гидравлическим дроссельным клапаном , кривая системы изменяется. 6.7 Дроссельный клапан Cummins работает с системой рециркуляции отработавших газов для рециркуляции отработавших газов через впускное отверстие за счет более низкого выброса трубы.
6.7 Дроссельный клапан Cummins работает с системой рециркуляции отработавших газов для рециркуляции отработавших газов через впускное отверстие за счет более низкого выброса трубы. 7 Дроссельный клапан Cummins
7 Дроссельный клапан Cummins Одним из таких клапанов является дроссельный клапан , который используется для регулирования количества воздуха, проходящего через двигатель. Клапан управления дроссельной заслонкой похож на педаль автомобиля. Он создает замкнутую систему управления, гарантирующую, что дроссельная заслонка открыта. Одно из преимуществ электронного обратного клапана дроссельной заслонки заключается в том, что его можно подключить к таким системам, как контроль тяги, управление двигателем, круиз-контроль и электронный контроль устойчивости. Производители дроссельной заслонки рекомендуют эти клапаны, поскольку другие системы могут при необходимости взять на себя управление дроссельной заслонкой, что повышает эффективность использования топлива, безопасность автомобиля и удобство.
Одним из таких клапанов является дроссельный клапан , который используется для регулирования количества воздуха, проходящего через двигатель. Клапан управления дроссельной заслонкой похож на педаль автомобиля. Он создает замкнутую систему управления, гарантирующую, что дроссельная заслонка открыта. Одно из преимуществ электронного обратного клапана дроссельной заслонки заключается в том, что его можно подключить к таким системам, как контроль тяги, управление двигателем, круиз-контроль и электронный контроль устойчивости. Производители дроссельной заслонки рекомендуют эти клапаны, поскольку другие системы могут при необходимости взять на себя управление дроссельной заслонкой, что повышает эффективность использования топлива, безопасность автомобиля и удобство. США / шт.
США / шт. 3D-демонстрация блока клапанов была построена и представлена для числового анализа с использованием ANSYS CFX. На основе характерной информации о приближении была проанализирована работа дисплея, и события отображаются в порядке, чтобы показать, как параметры изменяются при использовании дроссельных клапанов в контуре, управляемом давлением.
3D-демонстрация блока клапанов была построена и представлена для числового анализа с использованием ANSYS CFX. На основе характерной информации о приближении была проанализирована работа дисплея, и события отображаются в порядке, чтобы показать, как параметры изменяются при использовании дроссельных клапанов в контуре, управляемом давлением. таблицу
таблицу Скорость потока используется для управления работой клапанов управления потоком.
Скорость потока используется для управления работой клапанов управления потоком. /дюйм
/дюйм  Обычное использование — управление скоростью ствола или других приводов. Проверка свободного потока позволяет управлять исполнительным механизмом ввода или вывода расходомера.
Обычное использование — управление скоростью ствола или других приводов. Проверка свободного потока позволяет управлять исполнительным механизмом ввода или вывода расходомера.
 стартер, фара) 17/14 ,125cc, 2020г.
стартер, фара) 17/14 ,125cc, 2020г. сцепл., эл. стартер)
сцепл., эл. стартер)
 Закон о запрете продажи новой техники с ДВС должен был быть принят 7 марта 2023 года, однако,
Закон о запрете продажи новой техники с ДВС должен был быть принят 7 марта 2023 года, однако, Свяжитесь с нами сегодня и давайте поговорим о ваших требованиях к оборудованию
Свяжитесь с нами сегодня и давайте поговорим о ваших требованиях к оборудованию Свяжитесь с нами сегодня и давайте поговорим о ваших требованиях к оборудованию
Свяжитесь с нами сегодня и давайте поговорим о ваших требованиях к оборудованию Наша дистрибьюторская сеть, известная по всей стране, обслуживает более миллиона клиентов всех размеров, предлагая широкий ассортимент высококачественной продукции и непревзойденный опыт.
Наша дистрибьюторская сеть, известная по всей стране, обслуживает более миллиона клиентов всех размеров, предлагая широкий ассортимент высококачественной продукции и непревзойденный опыт. Устройство для выравнивания потока защитного газа на выходе из горелки для обеспечения оптимального охвата зоны сварки.
Устройство для выравнивания потока защитного газа на выходе из горелки для обеспечения оптимального охвата зоны сварки. Также называется сваркой MIG.
Также называется сваркой MIG.
